题目内容
13.在一密闭容器中充入3mol H2和1mol N2,在一定温度下使其发生反应,并达到平衡:3H2(g)+N2(g)?2NH3(g)△H<0;(填“不”、“正向”或“逆向”)(1)若保持容器容积不变:提高反应温度,平衡将逆向移动;
(2)若保持容器容积不变:向其中加入1molH2,平衡将正向移动;
(3)若保持容器容积不变:向其中加入1molNe(氖气),平衡将不移动;
(4)若保持容器容积不变:向其中加入1molHCl(气体),平衡将正向移动;
(5)若保持容器内气体压强不变:向其中加入铁触媒(催化剂),平衡将不移动;
(6)若保持容器内气体压强不变:向其中加入1molNe(氖气),平衡将逆向移动.
分析 (1)正反应是放热反应,提高反应温度,平衡向逆反应方向移动;
(2)增加反应物的浓度平衡正向移动;
(3)若保持容器容积不变:向其中加入1molNe(氖气),各物质的浓度不变,平衡不移动;
(4)若保持容器容积不变:向其中加入1molHCl(气体),氯化氢消耗氨气,生成物的浓度减少,平衡将正向移动;
(5)若保持容器内气体压强不变:向其中加入铁触媒(催化剂),使用催化剂平衡不移动;
(6)若保持容器内气体压强不变:向其中加入1molNe(氖气),体积变大,相当于体积不变,减小压强,平衡将正向移动.
解答 解:(1)正反应是放热反应,提高反应温度,平衡向吸热反应方向移动,即逆反应方向移动,故答案为:逆向;
(2)向其中加入1molH2,增加反应物的浓度平衡正向移动,故答案为:正向;
(3)若保持容器容积不变:向其中加入1molNe(氖气),各物质的浓度不变,平衡不移动,故答案为:不;
(4)若保持容器容积不变:向其中加入1molHCl(气体),氯化氢消耗氨气,生成物的浓度减少,平衡将正向移动,故答案为:正向;
(5)若保持容器内气体压强不变:向其中加入铁触媒(催化剂),使用催化剂平衡不移动,故答案为:不;
(6)若保持容器内气体压强不变:向其中加入1molNe(氖气),体积变大,相当于体积不变,减小压强,平衡将逆向移动,故答案为:逆向.
点评 本题考查化学平衡的影响因素,题目难度不大,本题注意浓度、压强对化学平衡的影响,把握浓度的变化转化为压强问题是解答的关键.

练习册系列答案
相关题目
4.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 标准状况下,以任意比例混合的甲烷和乙烯混合物22.4 L充分燃烧,生成物中水的分子数为2NA | |
| B. | 标准状况下,11.2L辛烷完全燃烧后,所生成气态产物的分子数为4NA | |
| C. | 常温常压下,1mol苯中含有3NA碳碳双键、3NA碳碳单键 | |
| D. | 常温常压下,1 mol甲烷和1mol氯气光照反应生成2NA个气体分子 |
8.如表离子组中所给离子在水溶液中能大量共存,且当加入试剂后反应的离子方程式书写完全且正确的是( )
| 选项 | 离子组 | 加入试剂 | 发生反应的离子方程式 |
| A | Fe3+、S2ˉ、Clˉ、Na+ | NaOH溶液 | Fe3++3OHˉ═Fe(OH)3↓ |
| B | H+、Fe2+、SO42ˉ、NO3ˉ | BaCl2溶液 | SO42ˉ+Ba2+═BaSO4↓ |
| C | Na+、Al3+、Clˉ、SO42ˉ | 少量KOH溶液 | Al3++3OHˉ═Al(OH)3↓ |
| D | Na+、K+、ClOˉ、SO42ˉ | 通入少量SO2 | 2ClOˉ+SO2+H2O═2HClO+SO32ˉ |
| A. | A | B. | B | C. | C | D. | D |
 铜是过渡金属元素,可以形成多种化合物.
铜是过渡金属元素,可以形成多种化合物.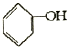 合成
合成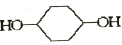 .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)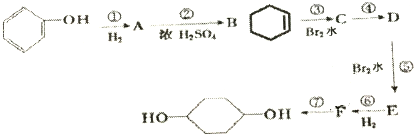
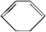 、E
、E .
.
 .
.