题目内容
3. 铜是过渡金属元素,可以形成多种化合物.
铜是过渡金属元素,可以形成多种化合物.(1)CuCl的盐酸溶液能够与CO发生反应:CuCl+CO+H2O═Cu(CO)Cl•H2O
①电负性:C<O(填“>”或“=”或“<”).
②CO常温下为气体,固态时属于分子晶体.
(2)Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s轨道及4p通过sp1杂化接受NH3提供的电子对.[Cu(NH3)n]+ 中Cu+ 与n个氮原子的空间结构呈直线 型,n=2.
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
请回答下列问题:
①该配离子[Cu(En)2]2+中的中心原子的基态外围电子排布式为3d9.
②乙二胺分子中氮原子轨道的杂化类型为sp3杂化,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键.
③该配离子[Cu(En)2]2+中存在的作用力类型有ABD(填字母);A.配位键 B.极性键 C.离子键
D.非极性键 E.氢键 F.金属键.
分析 (1)①同一周期元素从左到右电负性逐渐增大;②CO在常温下为气态,符合分子晶体的性质;
(2)Cu+有2个空的sp杂化轨道,NH3分子中的N原子有一孤电子对,进入Cu+空的sp杂化轨道,以配位键形成直线形结构;
(3)①根据核外电子排布规律书写Cu原子的核外电子排布式,电子按能层高低进行失去,进而书写Cu2+的外围电子排布式;
②乙二胺(H2N-CH2-CH2-NH2)中N原子呈3个σ键,含有1对孤对电子,杂化轨道数为4,采取sp3杂化;
乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,但三甲胺[N(CH3)3]分子之间不能形成氢键;
③离子中存在配位键、C-N键、C-H键、N-H键、C-C键,据此判断离子化学键类型.
解答 解:(1)①同一周期元素从左到右电负性逐渐增大,故电负性C<O,故答案为:<;
②CO在常温下为气态,符合分子晶体的性质,所以CO固态时是分子晶体,故答案为:分子;
(2)Cu+有2个空的sp杂化轨道,NH3分子中的N原子有一孤电子对,进入Cu+空的sp杂化轨道,以配位键形成直线形结构,则[Cu(NH3)n]+中Cu+与2个氮原子形成配位键,
故答案为:直线;2;
(3)①Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,故Cu2+的外围电子排布式为3d9,故答案为:3d9;
②乙二胺(H2N-CH2-CH2-NH2)中N原子呈3个σ键,含有1对孤对电子,杂化轨道数为4,采取sp3杂化;
乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高,
故答案为:sp3杂化;乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
③离子中存在配位键、C-N键、C-H键、N-H键、C-C键,其中C-N键、C-H键、N-H键为极性键,C-C键为非极性键,故离子含有配位键、极性键、非极性键,故选ABD.
故答案为:ABD.
点评 本题考查核外电子排布规律、杂化轨道、分子空间结构、氢键与化学键等,综合性较大,难度中等,是对知识的综合运用,需要学生具备扎实的基础与分析问题解决问题的能力.

 阅读快车系列答案
阅读快车系列答案| A. | 过滤法 | B. | 蒸馏法 | C. | 分液法 | D. | 萃取法 |
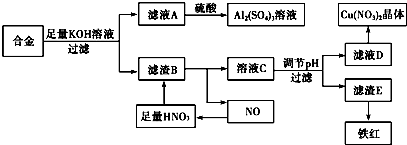
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)MnO4- 氧化Fe2+的离子方程式补充完整:1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:生成氢氧话务沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4- 可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
| A. | 2-甲基丙烷 正丁烷 | B. | 氧气 臭氧 | ||
| C. | 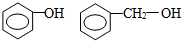 | D. | 金刚石 石墨 |

 如图是一个化学过程的示意图.已知甲池的总反应式为:
如图是一个化学过程的示意图.已知甲池的总反应式为: