题目内容
18.北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).(1)丙烷脱氢可得丙烯.
已知:C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ/mol
CH3CH=CH2(g)═CH4(g)+HC≡CH(g)△H2=+32.4kJ/mol
则相同条件下,反应C3H8(g)═CH3CH=CH2(g)+H2(g)的△H=+124.2kJ/mol.
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐.电池总反应方程式为C3H8+5O2=3CO2+4H2O;放电时CO32-移向电池的负(填“正”或“负”)极.
(3)常温下,0.1mol/LNaHCO3溶液的pH大于8,则溶液中c(H2CO3)>c(CO32-)(填“>”、“=”或“<”),原因是HCO3-?CO32-+H+、HCO3-+H2O?H2CO3+OH-,HCO3-的水解程度大于电离程度(用离子方程式和必要的文字说明).
分析 (1)根据已知反应和目标反应,利用盖斯定律可知反应C3H8(g)→CH3CH=CH2(g)+H2(g)由已知的反应相减得到,则△H=△H1-△H2;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,以此来书写电池总反应方程式,原电池中阴离子向负极移动;
(3)NaHCO3溶液的pH大于8,则水解大于电离,水解生成H2CO3,电离生成CO32-.
解答 解:(1)由C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ•mol-1①,
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ•mol-1 ②,
则根据盖斯定律,反应C3H8(g)→CH3CH=CH2(g)+H2(g)可由①-②得到,
所以△H=△H1-△H2=+156.6kJ•mol-1-(+32.4kJ•mol-1)=+124.2kJ•mol-1,
故答案为:+124.2;
(2)负极通入丙烷,碳元素的化合价升高,电池的正极通入O2,氧元素的化合价降低,即丙烷与氧气反应生成二氧化碳和水,
则电池的总反应为C3H8+5O2═3CO2+4H2O,原电池中阴离子向负极移动,即CO32-移向电池的负极,
故答案为:C3H8+5O2═3CO2+4H2O;负;
(3)NaHCO3溶液的pH大于8,则水解大于电离,水解生成H2CO3,电离生成CO32-,即HCO3-?CO32-+H+,HCO3-+H2O?H2CO3+OH-,所以c(H2CO3)>c(CO32-),HCO3-的水解程度大于电离程度,
故答案为:>; HCO3-?CO32-+H+、HCO3-+H2O?H2CO3+OH-,HCO3-的水解程度大于电离程度.
点评 本题考查了多个知识点,属于小综合习题,明确盖斯定律、原电池的工作原理、电离平衡常数的计算、溶液中利用电离与水解来比较离子的浓度即可解答,难度中等.

| A. | 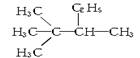 与 与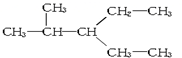 | B. | 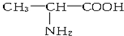 与CH3-CH2-CH2-NO2 与CH3-CH2-CH2-NO2 | ||
| C. | CH3COOCH2CH3与CH3CH2COOH | D. | C2H5-O-C2H5与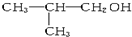 |
| A. | 由甲苯制甲基环己烷、由乙烷制溴乙烷 | |
| B. | 乙烯使溴水褪色、乙炔使酸性高锰酸钾水溶液褪色 | |
| C. | 由乙烯制聚乙烯、由氯乙烯制聚氯乙烯 | |
| D. | 由苯制硝基苯、由溴乙烷制取乙醇 |

| A. | 有机物E的名称是异丙烷 | B. | B与C及D毒为同分异构体 | ||
| C. | F与G互为同系物 | D. | A与H实验式相同 |
| A. | v(NH3)=0.6 mol•L-1•min-1 | B. | v(N2)=0.005 mol•L-1•s-1 | ||
| C. | v(H2)=0.9 mol•L-1•min-1 | D. | v(NH3)=0.02 mol•L-1•s-1 |
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)═SO2(g)△H=-269.8kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | NH3•H2O(aq)+HCl(aq)═NH4Cl(aq)+H2O(l)△H=-57.3kJ/mol(中和热) |
| A. | 将铝表面的氧化物溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3↓ | |
| B. | 碳酸氢钠的水解:HCO3-+H2O?H3O++CO32- | |
| C. | 500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g).放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6KJ/mol | |
| D. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=-890.3kJ•mol-1 |