��Ŀ����
����Ŀ��������һ����Ҫ�Ļ�����Ʒ��
(1)��ҵ����������������һ�������ºϳɰ������йط���ʽ���£� 3H2 (g)+N2(g)2NH3 (g) + 92.4 kJ
�ٶ��ڸ÷�Ӧ��Ҫʹ��Ӧ�ᄀ���ܿ��ת��Ϊ�������ɲ��õķ�Ӧ������__________��Ҫʹ��Ӧ�ᄀ���ܶ��ת��Ϊ�������ɲ��õķ�Ӧ������__________��(��ѡ����ĸ)
A���ϸ��¶�B���ϵ��¶�C���ϸ�ѹǿ D���ϵ�ѹǿ E��ʹ�ú��ʵĴ���
��ҵ�϶Ժϳɰ����˷�Ӧ����ѡ�����ۺϿ����˻�ѧ��Ӧ���ʡ���ѧƽ����豸���ϵȵ�Ӱ�졣
�ڸ÷�Ӧ�ﵽƽ���ֻ�ı�����һ�����أ����·����в���ȷ����_______��(ѡ����ĸ)
A�������¶ȣ�������Ӧ�ķ�Ӧ����Ӱ�����
B������ѹǿ��������Ӧ�ķ�Ӧ����Ӱ�����
C����С������Ũ�ȣ����淴Ӧ�ķ�Ӧ����Ӱ�����
��ij������Ϊ���ۺ��������������и���ƷCaSO4�������ڵĺϳɰ�������������Ʊ�(NH4)2SO4�Ĺ�������(��ͼ)���������У�
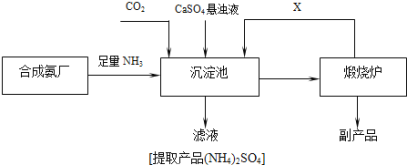
���������ͨ�������İ�����Ŀ����______________________________������ѭ��ʹ�õ�X��_______________��(�ѧʽ)
(2)ʵ�����п����������ǿ��ȵõ��������йص����ӷ���ʽΪ_____________________��
��0.01 mol/L�������Һ0.5L��������������������Һ���ȣ��ɲ�������_____L(��״̬)��
����������狀�����淋Ļ����Һ0.5L��������������������Һ���ȣ��ɲ�������0.025mol���ڷ�Ӧ�����Һ�м����������Ȼ�����Һ������0.01 mol ��ɫ��������ԭ���Һ�У�����淋�Ũ��Ϊ_______mol/L��
����������李��Ȼ�狀�����淋Ļ����ҺV L���������Һ�ֳ����ȷ֣�һ����Һ������������������Һ���ȣ�����������A mol����һ����Һ����������C mol/L���Ȼ�����ҺB L����Һ��SO42-ǡ��ȫ�����������������˺�����Һ�м���������������Һ���������ֲ���D mol��������ԭ�����Һ�У��Ȼ�淋�Ũ��Ϊ________mol/L������淋�Ũ��Ϊ_______mol/L��(�ú�����ĸ�Ĵ���ʽ��ʾ)
���𰸡�ACE BC A �������Σ�ʹCa2+��ȫ���� CO2 NH4++OH-![]() H2O+NH3
H2O+NH3![]() 0.112 0.01
0.112 0.01 ![]()
![]()
��������
(1)��Ҫʹ��Ӧ�ᄀ���ܿ��ת��Ϊ��������Ҫ�ӿ췴Ӧ���ʣ�����ͨ�������¶ȡ�����ѹǿ��ʹ�ú��ʵĴ���ʵ�֣�Ҫʹ��Ӧ�ᄀ���ܶ��ת��Ϊ��������Ҫ��Ӧ�����ƶ�����Ӧ3H2 (g)+N2(g)2NH3 (g) + 92.4 kJ�����������С�ķ��ȷ�Ӧ������ͨ������ѹǿ�ͽϵ��¶�ʵ�֣�
�ڸ���Ӱ��ƽ���ƶ������������жϣ�
�����������̵ij�������ͨ������������Ŀ����һ�����ṩ��Ӧ���һ����ʹ��Һ�ʼ���������CO2�����գ�������¯�з���CaCO3![]() CaO+CO2������XΪCO2���ڴ��Ʊ�ʵ����ѭ��ʹ�ã�
CaO+CO2������XΪCO2���ڴ��Ʊ�ʵ����ѭ��ʹ�ã�
(2)�����ǿ��ȵõ�������ˮ��
�ٸ���NH4+Ԫ���غ���㣻
�ڸ���NH4+Ԫ���غ���㣻��
��һ����Һ������������������Һ���ȣ�����������A mol������NH4++OH-�TNH3+H2O��֪ÿ���к���AmolNH4+�����Ȼ�����Һ��ȫ��Ӧ����C mol/LBaCl2��ҺB L������Ba2++SO42-�TBaSO4����֪ÿ�ݺ���SO42-CBmol�����������˺�����Һ�м���������������Һ���������ֲ���D mol����������Ag++Cl-=AgCl�������ǰ�����CBmol��BaCl2��Һ��֪��ÿ�ݺ���Cl-(D-2BC) mol��
(1)��Ҫʹ��Ӧ�ᄀ���ܿ��ת��Ϊ��������Ҫ�ӿ췴Ӧ���ʣ�����ͨ�������¶ȡ�����ѹǿ��ʹ�ú��ʵĴ���ʵ�֣���ѡACE��Ҫʹ��Ӧ�ᄀ���ܶ��ת��Ϊ��������Ҫ��Ӧ�����ƶ�����Ӧ3H2 (g)+N2(g)2NH3 (g) + 92.4 kJ�����������С�ķ��ȷ�Ӧ������ͨ������ѹǿ�ͽϵ��¶�ʵ�֣���ѡBC��
��A. ��Ӧ3H2 (g)+N2(g)2NH3 (g) + 92.4 kJ�����������С�ķ��ȷ�Ӧ�������¶ȷ�Ӧ�����ƶ���˵�������¶ȣ����淴Ӧ�ķ�Ӧ����Ӱ�����A����
B. ��Ӧ3H2 (g)+N2(g)2NH3 (g) + 92.4 kJ�����������С�ķ��ȷ�Ӧ������ѹǿ��Ӧ���ʼӿ죬��Ӧ�����ƶ���˵������ѹǿ������Ӧ�ķ�Ӧ����Ӱ�����B��ȷ��
C. ��С������Ũ�ȣ���Ӧ�����ƶ���˵����С������Ũ�ȶ��淴Ӧ�ķ�Ӧ����Ӱ�����C��ȷ��
��ѡA��
�����������̵ij�������ͨ������������Ŀ����һ�����ṩ��Ӧ���һ����ʹ��Һ�ʼ���������CO2�����գ�������¯�з���CaCO3![]() CaO+CO2������XΪCO2���ڴ��Ʊ�ʵ����ѭ��ʹ�ã�
CaO+CO2������XΪCO2���ڴ��Ʊ�ʵ����ѭ��ʹ�ã�
(2)�����ǿ��ȵõ�������ˮ�����ӷ���ʽΪ��NH4++OH-![]() H2O+NH3
H2O+NH3![]() ��
��
��0.5L 0.01 mol/L�������Һ������淋����ʵ���Ϊ��0.5L![]() 0.01 mol/L=0.005mol������NH4+�غ㣬������ɰ���0.005mol������µ����Ϊ��0.005mol
0.01 mol/L=0.005mol������NH4+�غ㣬������ɰ���0.005mol������µ����Ϊ��0.005mol![]() 22.4L/mol=0.112L��
22.4L/mol=0.112L��
���������֪���ڷ�Ӧ�����Һ�м����������Ȼ�����Һ������0.01 mol BaSO4��ɫ������˵��ԭ��Һ�к��������0.01mol��������淋����ʵ���Ϊxmol������NH4+�غ���x+0.01mol![]() 2=0.025����x=0.005mol������淋�Ũ��Ϊ
2=0.025����x=0.005mol������淋�Ũ��Ϊ![]() =0.01mol/L��
=0.01mol/L��
��һ����Һ������������������Һ���ȣ�����������A mol������NH4++OH![]() mol/L =
mol/L =![]() mol/L��ÿ��������������ʵ���Ϊ�� n(NH4+)- n(Cl-)-2n(SO42-)=
mol/L��ÿ��������������ʵ���Ϊ�� n(NH4+)- n(Cl-)-2n(SO42-)=![]() ������淋�Ũ��Ϊ
������淋�Ũ��Ϊ![]() mol/L =
mol/L = ![]() mol/L��
mol/L��

����Ŀ�������й�ʵ�����������ͽ��۶���ȷ���ǣ� ��
ѡ�� | ʵ����� | ���� | ���� |
A | ϡ������Һ�м���������۳�ַ�Ӧ�μ�KSCN��Һ | ��Һ��ΪѪ��ɫ | ϡ������������ԣ��ܽ�Fe������Fe3+ |
B | ��AgNO3��Һ�еμӹ�����ˮ | ��Һ���� | Ag+��NH3��H2O�ܴ������� |
C | ��ij��Һ�еμ�ϡNaOH��Һ����ʪ��ĺ�ɫʯ����ֽ�����Թܿ� | ��ֽ���� | ����Һ�д���NH4+ |
D | ���з�̪��Na2CO3��Һ�м���������BaCl2���� | ��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
A. AB. BC. CD. D