题目内容
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
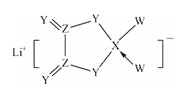
A.32 g S8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
B.1L、0.1mol/L的Na2CO3溶液中含阴离子总数为0.1NA个
C.标准状况下,22.4LHF含NA个分子
D.标准状况下,11.2 L Cl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA
【答案】A
【解析】
A. S8分子结构:![]() ,1个分子含有8个共价键, 32 g S8物质的量为0.125mol,因此32 g S8中的共价键数目为NA,故A正确;
,1个分子含有8个共价键, 32 g S8物质的量为0.125mol,因此32 g S8中的共价键数目为NA,故A正确;
B. 1L、0.1 molL1的Na2CO3溶液中碳酸根物质的量为0.1mol,碳酸根水解生成碳酸氢根和氢氧根,因此溶液中含阴离子总数大于0.1NA个,故B错误;
C. HF在标准状况下是非气态的物质,无法计算物质的量,故C错误;
D. 标准状况下,11.2 L Cl2物质的量为0.5mol,0.5mol Cl2 溶于水是可逆反应,因此溶液中Cl-、ClO-和HClO的微粒数之和小于NA,故D错误。
综上所述,答案为A。

 优等生题库系列答案
优等生题库系列答案【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
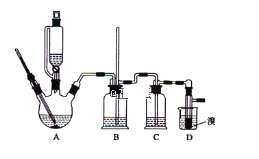
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)写出由乙醇制备乙烯的化学方程式______________________________,乙烯制备1,2-二溴乙烷的化学方程式_______________________________。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___________;(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置A中除了浓硫酸和乙醇外,还应加入_____,其目的是_______装置A中生成副产物乙醚的化学反应方程式 ___________________。
(4)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放 ________________,
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液d.品红和酸性KMnO4
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_______的方法除去。