��Ŀ����
6��A��B��C��D��E��F�Ǻ˵������������Ķ���������Ԫ�أ�Ԫ��A��ԭ�Ӻ���û�����ӣ�A��D������������ȣ�B��Cͬ���ڣ�C��Fͬ���壬F��������ΪC��2����Ԫ��B����������Ϊ��ɫֲ����й�����õı������ʣ�D��E��F������������Ӧ��ˮ��������֮�������Ӧ����1��д��F�����ڱ��е�λ�õ������ڢ�A�壻B��ԭ�ӽṹʾ��ͼ
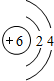
��2����C��D��ɵ�һ�ֻ��������ԭ�Ӹ�����Ϊ1��1��д�����ĵ���ʽ
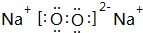 �����ڵĻ�ѧ�����������Ӽ������ۼ��������Ӧ�Ļ�ѧ����ʽ��2Na2O2+2CO2=2Na2CO3+O2��
�����ڵĻ�ѧ�����������Ӽ������ۼ��������Ӧ�Ļ�ѧ����ʽ��2Na2O2+2CO2=2Na2CO3+O2����3���Ƚ�C��F��D�����Ӱ뾶�Ĵ�СS2-��O2-��Na+�������ӷ��ű�ʾ��
��4��D��E������������Ӧ��ˮ����֮�䷴Ӧ�����ӷ���ʽΪAl��OH��3+OH-=AlO2-+2H2O��
��5��A2C��A2F�У��е�ϸߵ���A2C��ԭ����H2O����֮����������H2S����֮��Ϊ���»���������ȷ��»�����ǿ��
���� A��B��C��D��E��F�Ǻ˵������������Ķ���������Ԫ�أ�Ԫ��A��ԭ�Ӻ���û�����ӣ���AΪHԪ�أ�A��D������������ȣ�����ͬ���壬ԭ������������2����DΪNa��D��E��F������������Ӧ��ˮ��������֮�������Ӧ����ԭ��������֪�����ڵ������ڣ�Ӧ������������ǿ�ǿ��ķ�Ӧ����EΪAl��B��Cͬ���ڣ�ԭ��������С���ƣ��ʶ��ߴ��ڵڶ����ڣ�C��Fͬ���壬F��������ΪC��2������CΪOԪ�ء�FΪSԪ�أ�Ԫ��B����������Ϊ��ɫֲ����й�����õı������ʣ���BΪ̼Ԫ�أ���ΪCO2���ݴ˽��
��� �⣺A��B��C��D��E��F�Ǻ˵������������Ķ���������Ԫ�أ�Ԫ��A��ԭ�Ӻ���û�����ӣ���AΪHԪ�أ�A��D������������ȣ�����ͬ���壬ԭ������������2����DΪNa��D��E��F������������Ӧ��ˮ��������֮�������Ӧ����ԭ��������֪�����ڵ������ڣ�Ӧ������������ǿ�ǿ��ķ�Ӧ����EΪAl��B��Cͬ���ڣ�ԭ��������С���ƣ��ʶ��ߴ��ڵڶ����ڣ�C��Fͬ���壬F��������ΪC��2������CΪOԪ�ء�FΪSԪ�أ�Ԫ��B����������Ϊ��ɫֲ����й�����õı������ʣ���BΪ̼Ԫ�أ���ΪCO2��
��1��FΪSԪ�أ������ڱ��е�λ�ã��������ڢ�A�壻BΪ̼Ԫ�أ�ԭ�ӽṹʾ��ͼΪ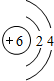 ��
��
�ʴ�Ϊ���������ڢ�A�壻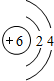 ��
��
��2����C��D��ɵ�һ�ֻ��������ԭ�Ӹ�����Ϊ1��1�����ΪNa2O2������ʽΪ ���������Ӽ������ۼ�����ף�������̼����Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2CO2=2Na2CO3+O2��
���������Ӽ������ۼ�����ף�������̼����Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2CO2=2Na2CO3+O2��
�ʴ�Ϊ�� �����Ӽ������ۼ���2Na2O2+2CO2=2Na2CO3+O2��
�����Ӽ������ۼ���2Na2O2+2CO2=2Na2CO3+O2��
��3�����ӵĵ��Ӳ���Խ�࣬�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�������У����Ӱ뾶����ԭ���������������С���������Ӱ뾶��С˳����S2-��O2-��Na+��
�ʴ�Ϊ��S2-��O2-��Na+��
��4��D��E������������Ӧ��ˮ����ֱ�ΪNaOH��Al��OH��3�����߷�Ӧ���ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��5������H2O����֮����������H2S����֮��Ϊ���»���������ȷ��»�����ǿ����ˮ�ķе����H2S��
�ʴ�Ϊ��H2O����֮����������H2S����֮��Ϊ���»���������ȷ��»�����ǿ��
���� ���⿼��λ�ýṹ���ʹ�ϵ����Ӧ�ã��ƶ�Ԫ���ǽ���ؼ���ע��������������ʵ�Ӱ�죬ע��Ի���֪ʶ���������գ�

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�| A�� | �Ҵ�������ˮ���������л��ܼ� | |
| B�� | ���ķ��ӽṹ�к���̼̼˫�� | |
| C�� | ��ϩͨ������KMn04��Һ�У���ɫ��ȥ | |
| D�� | ������������ϩʹ�������������Һ��ɫ�ķ�Ӧ������ȡ����Ӧ |
| A�� | ʵ��ʣ���ҩƷ���ܷŻ�ԭ�Լ�ƿ | B�� | �ƾ����ھƾ��������ڵ��ݻ�$\frac{1}{4}$ | ||
| C�� | ʵ��������Թ���ϴ�ɾ� | D�� | ��ͷ�ιܲ��ܽ���ʹ�� |
| A�� | �ڽ����뺣�����γ������� | |
| B�� | ����ˮ��������������������ʹˮ��ó��� | |
| C�� | ��NaCl��Һ�е���AgNO3��Һ��������ɫ���� | |
| D�� | ͬһ�ֱ�ͬʱʹ�ò�ͬ�ƺŵ�īˮ�������� |

 ClO2������һ�ֳ��õ����������������ҹ���ClO2��������������ˮ����������
ClO2������һ�ֳ��õ����������������ҹ���ClO2��������������ˮ����������