题目内容
6.下列说法中正确的是( )| A. | 1mol•L-1的NaCl溶液是指此溶液中含有1mol NaCl | |
| B. | 从1L0.5mol•L-1的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol/L | |
| C. | 25℃时,1mol Cl2的体积约为22.4L | |
| D. | 1mol•L-1的CaCl2溶液中,Cl-的物质的量浓度为2 mol/L |
分析 A.根据物质的量浓度概念分析;
B.溶液是均一稳定的混合物;
C.不是标准状况下,不能使用标准状况下的气体摩尔体积计算;
D.根据电解质浓度和离子浓度关系分析.
解答 解:A.1mol/L的NaCl溶液是指此1L溶液中含有1mol NaCl,若溶液体积是0.5L,则含氯化钠为0.5ml,故A错误;
B.溶液是均一稳定的混合物,故从1 L 0.5 mol/L的NaCl溶液中取出100 mL溶液,其物质的量浓度仍为0.5 mol/L,故B错误;
C.标况下,气体摩尔体积为22.4L/mol,1molCl2的体积约为22.4L,25℃时大于22.4L,故C错误;
D.氯离子浓度为氯化钙浓度的2倍,则Cl-的物质的量浓度为2 mol/L,故D正确;
故选D.
点评 本题考查了物质的量浓度的计算与判断,题目难度中等,注意对公式的理解与灵活运用,注意根据化学式计算电解质离子浓度与电解质的浓度关系,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
16.研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)═2Fe (s)+3CO(g)△H1=+489.0kJ•mol-1,
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1,则CO还原Fe2O3(s)的热化学方程式为Fe2O3 (s)+3CO(g)=2Fe(s)+3CO2 (g)△H=-28.5kJ•mol-1.
(2)CO与O2设计成燃料电池(以KOH溶液为电解液).该电池的负极反应式为CO+4OH--2e-=CO32-+2H2O.
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g) 测得CH3OH的物质的量随时间的变化如图1.
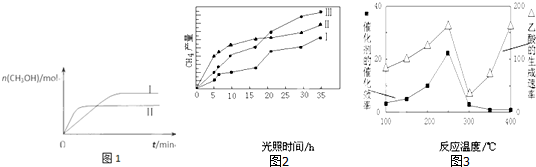
①该反应的△H>0(填“大于或小于”),曲线I、Ⅱ对应的平衡常数大小关系为KⅠ<KⅡ(填“>、=或<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为0.4<b≤1.
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图2.在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为II>III>I(填序号).
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图3.
①当温度在300℃~400℃范围时,温度是乙酸生成速率的主要影响因素.
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O.
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)═2Fe (s)+3CO(g)△H1=+489.0kJ•mol-1,
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1,则CO还原Fe2O3(s)的热化学方程式为Fe2O3 (s)+3CO(g)=2Fe(s)+3CO2 (g)△H=-28.5kJ•mol-1.
(2)CO与O2设计成燃料电池(以KOH溶液为电解液).该电池的负极反应式为CO+4OH--2e-=CO32-+2H2O.
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g) 测得CH3OH的物质的量随时间的变化如图1.

①该反应的△H>0(填“大于或小于”),曲线I、Ⅱ对应的平衡常数大小关系为KⅠ<KⅡ(填“>、=或<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3mol H2 | a molCO2、3a molH2、 b molCH3OH(g)、b molH2O(g) |
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图2.在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为II>III>I(填序号).
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图3.
①当温度在300℃~400℃范围时,温度是乙酸生成速率的主要影响因素.
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O.
1.某烃的结构简式为CH≡C-C(C2H5)═CH-CH2-CH3分子中处于四面体结构中心的碳原子(即饱和碳原子)数为a,一定在同一直线上的碳原子数为b,一定在同一平面内的碳原子数为c,则a,b,c分别为( )
| A. | 4,3,5 | B. | 2,5,4 | C. | 4,3,6 | D. | 4,4,6 |
11.已知Co2O3在酸性溶液中易被还原成Co2+;则Co2O3、Cl2、FeCl3、I2的氧化性依次减弱.下列反应在水溶液中不可能发生的是( )
| A. | Cl2+2FeCl2═2FeCl3 | B. | 3I2+6FeCl2═4FeCl3+2FeI3 | ||
| C. | Co2O3+6HCl═2CoCl2+Cl2↑+3H2O | D. | 2Fe3++2I-═2Fe2++I2 |
18.从下列实验事实所得出的相应结论正确的是( )
| 选项 | 实验事实 | 结论 |
| A | Na2S2O3溶液与稀硫酸反应,其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度,化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生变化 | 催化剂一定不参与化学反 应 |
| C | H+浓度相同的盐酸和醋酸分别与等质量的形状相同的锌反应 | 前者速率快 |
| D | 在容积可变的密闭容器中发生反应H2(g)+I2(g) 2HI(g),把容积缩小一半 | 正反应速率加快,逆反应速率不变 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关物质的性质与应用正确且相对应的是( )
| A. | Na、K合金熔点低、沸点高,可用作原子反应堆导热液 | |
| B. | SiO2具有高沸点,可用作制备光导纤维 | |
| C. | NH3具有还原性,可用作制冷剂 | |
| D. | HF是强酸,可用于雕刻玻璃 |
16.在2L容器中发生3A+B?2C的反应,最初加入的A、B都是4mol,若10s 后反应达到平衡,测得A的平均反应速率为0.15mol•L-1•s-1,则10s后容器内B的物质的量为( )
| A. | 1.5 mol | B. | 1.0 mol | C. | 3.0 mol | D. | 2.4 mol |
 .
.