题目内容
2.下列图示的实验操作不能实现相应实验目的是( )| A. |  证明装置的气密性良好 | |
| B. | 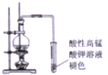 证明乙醇与浓H2SO4共热生成了大量乙烯 | |
| C. |  证明SO2有还原性 | |
| D. |  用饱和食盐水与CaC2制备并收集C2H2 |
分析 A.利用液差法检验气密性;
B.乙醇与浓H2SO4共热发生消去反应生成乙烯,乙醇易挥发,均能被高锰酸钾氧化;
C.白色沉淀为硫酸钡;
D.饱和食盐水与CaC2反应生成乙炔,且乙炔不溶于水.
解答 解:A.关闭止水夹,当长颈漏斗中液面高于烧瓶中液面,且一段时间不变,则气密性良好,故A正确;
B.乙醇与浓H2SO4共热发生消去反应生成乙烯,乙醇易挥发,均能被高锰酸钾氧化,应除去乙醇的干扰,故B错误;
C.白色沉淀为硫酸钡,可知二氧化硫与硝酸根离子发生氧化还原反应生成硫酸根离子,证明SO2有还原性,故C正确;
D.饱和食盐水与CaC2反应生成乙炔,且乙炔不溶于水,则图中装置可制备并收集C2H2,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及气密性检验、有机物的制备及检验、氧化还原反应等,把握物质的性质及化学反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.碱性电池有容量大,放电电流大的特点,被广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn+2MnO2+H2O=Zn(OH)2+Mn2O3.下列说法错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为2MnO2+H2O+2e-═Mn2O3+2OH- | |
| C. | 外电路中每通过0.2mol电子,锌的质量理论上减少13g | |
| D. | 电池工作时,电子由负极通过外电路流向正极 |
13.有两组物质:①组CH4、聚乙烯、邻二甲苯 ②组2-丁烯、乙炔、苯乙烯下列有关上述有机物说法正确的是
( )
( )
| A. | ①组物质都不能使酸性高锰酸钾褪色,②组物质都能使酸性高锰酸钾褪色 | |
| B. | ①组物质都不能使溴的四氯化碳褪色,②组物质都能使溴的四氯化碳褪色 | |
| C. | ②组物质所有原子可以在同一平面内 | |
| D. | 邻二甲苯的一氯代物只有两种 |
10.加入铝粉有氢气产生的溶液中,可能大量共存的离子组是( )
| A. | Ba2+、Na+、I-、Fe3+ | B. | Mg2+、Cl-、NO3-、Al3+ | ||
| C. | K+、Cl-、HCO3-、SO42- | D. | Ba2+、Na+、Cl-、[Al(OH)4]- |
17.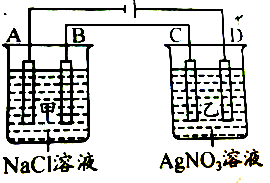 甲、乙两个容器中,分别加入0.1 mol•L -1的 NaCl溶液与0.1 mol•L-1的AgNO3溶液后,以 Pt为电极进行电解时,在A、B、C、D各电极上生成物的物质的量之比为 ( )
甲、乙两个容器中,分别加入0.1 mol•L -1的 NaCl溶液与0.1 mol•L-1的AgNO3溶液后,以 Pt为电极进行电解时,在A、B、C、D各电极上生成物的物质的量之比为 ( )
 甲、乙两个容器中,分别加入0.1 mol•L -1的 NaCl溶液与0.1 mol•L-1的AgNO3溶液后,以 Pt为电极进行电解时,在A、B、C、D各电极上生成物的物质的量之比为 ( )
甲、乙两个容器中,分别加入0.1 mol•L -1的 NaCl溶液与0.1 mol•L-1的AgNO3溶液后,以 Pt为电极进行电解时,在A、B、C、D各电极上生成物的物质的量之比为 ( )| A. | 2:2:4:1 | B. | 2:3:4:1 | C. | 1:4:2:2 | D. | 1:1:1:1 |
11.X、Y、R、M均为短周期元素,X、Y同周期,X、Y两种元素最高价氧化物对应水化物化学式分别为H2X04和HY04.R、M同主族,R与冷水即可反应,M与热水反应缓慢.下列关系正确的是( )
| A. | 原子半径X>Y | B. | 氢化物稳定性H2X>HY | ||
| C. | 原子核内质子数R<M | D. | 溶液碱性ROH<MOH |
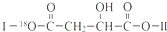 (其中Ⅰ、Ⅱ为未知部分的结构).下列是X发生反应的转化关系图及E的信息.
(其中Ⅰ、Ⅱ为未知部分的结构).下列是X发生反应的转化关系图及E的信息.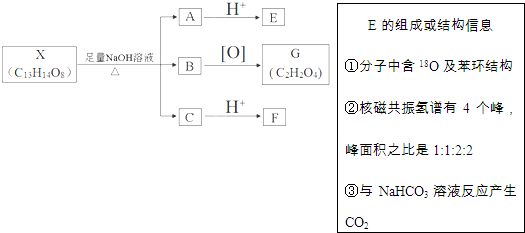
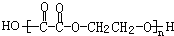 +(2n-1)H2O
+(2n-1)H2O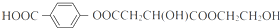 +4NaOH$→_{△}^{水}$
+4NaOH$→_{△}^{水}$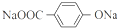 +NaOOCCH2CH(OH)COOONa+HOCH2CH2OH+2H2O
+NaOOCCH2CH(OH)COOONa+HOCH2CH2OH+2H2O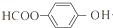 等
等
 -
-