题目内容
13.有两组物质:①组CH4、聚乙烯、邻二甲苯 ②组2-丁烯、乙炔、苯乙烯下列有关上述有机物说法正确的是( )
| A. | ①组物质都不能使酸性高锰酸钾褪色,②组物质都能使酸性高锰酸钾褪色 | |
| B. | ①组物质都不能使溴的四氯化碳褪色,②组物质都能使溴的四氯化碳褪色 | |
| C. | ②组物质所有原子可以在同一平面内 | |
| D. | 邻二甲苯的一氯代物只有两种 |
分析 A、苯的同系物,可以使酸性高锰酸钾溶液褪色;
B、含有不饱和双键或三键的能使溴水褪色;
C、依据甲烷、乙烯、乙炔以及苯的结构判断即可;
D、苯的同系物氯代物可以是苯环上的取代,也可以是烃基上的取代,据此解答即可.
解答 解:A、①组物质中邻二甲苯能使酸性高锰酸钾溶液褪色,故A错误;
B、①组物质中均为单键,不能使溴水褪色,②组物质中均含有不饱和键,能使溴水褪色,故B正确;
C、2-丁烯中含有2个甲基,甲基中的三个H原子与剩余的基团处于四面体位置,故不可能处于同一平面,故C错误;
D、邻二甲苯,苯环上的一氯代物只有2种,分别位于邻位和间位,两个甲基上可以生成1种一氯代物,故总共3种,故D错误,故选B.
点评 本题主要考查的是饱和烃与不饱和烃的性质、同分异构体个数判断、分子结构(共平面)等知识,综合性较强,但是难度不大.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
1.下列说法中正确的是( )
| A. | 饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 | |
| B. | AgCl悬浊液中存在平衡:AgCl(s)═Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 | |
| C. | AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI) | |
| D. | 硬水中含有较多的Ca2+?Mg2+?HCO3-、SO42-,加热煮沸可以完全除去其中的Ca2+?Mg2+ |
8.实验室测定溶液中RO3-浓度的方法之一是:取25mL待测液于锥形瓶中,加入足量的KI溶液,发生反应①.充分反应后,往锥形瓶中滴入2-3滴淀粉溶液,用0.001mol/L的Na2S2O3溶液滴定,发生反应②.反应方程式如下:
反应①aRO3-+bI-+cH+=dR-+eI2+fH2O
反应②I2+2Na2S2O3=2NaI+Na2S4O6
下列说法正确的是( )
反应①aRO3-+bI-+cH+=dR-+eI2+fH2O
反应②I2+2Na2S2O3=2NaI+Na2S4O6
下列说法正确的是( )
| A. | b=c | |
| B. | R元素位于周期表的ⅤA族 | |
| C. | 滴定终点时,溶液的颜色由无色变为蓝色 | |
| D. | 若滴定消耗Na2S2O3溶液20.00mL,则反应①转移电子6.02×1020个 |
18.用酸性氢氧燃料电池(甲池)为电源进行电解的实验装置(乙池,一定条件下可实现有机物的电化学储氢)如图所示.甲池中C为含苯的物质的量分数为10%的混合气体,D为l0mol混合气体其中苯的物质的量分数为24%(杂质不参与反应),E为标准状况下2.8mol气体(忽略水蒸汽),下列说法正确的是( )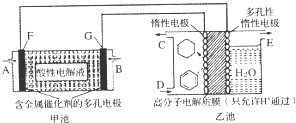

| A. | 甲池中A处通入H2,E处有O2放出 | B. | 甲池中H+由F极移向G极 | ||
| C. | 乙池中阴极区只有苯被还原 | D. | 导线中共传导11.2mol电子 |
5.下列有关电解质溶液的说法正确的是( )
| A. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 | |
| B. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 | |
| C. | 在Na2C2O4稀溶液中,c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| D. | 0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合:3c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] |
2.下列图示的实验操作不能实现相应实验目的是( )
| A. |  证明装置的气密性良好 | |
| B. | 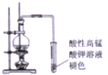 证明乙醇与浓H2SO4共热生成了大量乙烯 | |
| C. |  证明SO2有还原性 | |
| D. |  用饱和食盐水与CaC2制备并收集C2H2 |
3.只用一种试剂即可鉴别乙醇、乙醛、乙酸、甲酸等有机物的溶液,这种试剂是( )
| A. | 新制生石灰 | B. | 新制氢氧化铜 | C. | 浓溴水 | D. | 银氨溶液 |
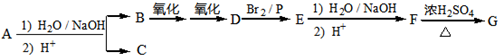

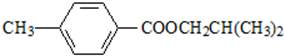 .
. ,该反应属于取代反应(或酯化反应)(填反应类型).
,该反应属于取代反应(或酯化反应)(填反应类型).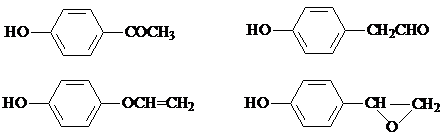 .
.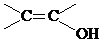 )结构.
)结构.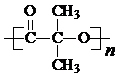 .
.