题目内容
【题目】实验室需要配制0.50 mol/L NaCl溶液 240 mL,现使用NaCl固体配制, 按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平 药匙、烧杯、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________g。
(3)称量。天平调平之后,应将天平的游码调至某个位置,请在下图中用一根 竖线标出游码左边缘所处的位置:______________
![]()
(4)将药品倒入烧杯中溶解、冷却。
(5)转移、洗涤。在转移时应使用玻璃棒引流,需要洗涤烧杯和玻璃棒2~3次是为了______________
(6)定容、摇匀。
(7)将配好的溶液倒入指定的试剂瓶,并贴好标签,注明溶液名称及浓度。
(8)配制时下列操作会导致所配溶液浓度偏高的是________。
A.转移时有少量溶液溅出 B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度 D.定容时液面超过了刻度线
E.称量NaCl时用了生锈的砝码
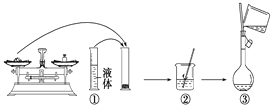
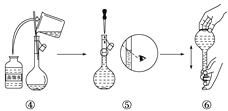
(9)下图是某同学在实验室配制该NaCl溶液的过程示意图,其中有错误的是________(填操作序号)。
【答案】 250 mL容量瓶 胶头滴管 7.3 ![]() 保证溶质全部转移到容量瓶中 CE ①③⑤
保证溶质全部转移到容量瓶中 CE ①③⑤
【解析】试题分析:(1)根据配制一定物质的量浓度溶液的一般步骤,用到的仪器有:托盘天平(精确到0.1g)、药匙、等质量的两片滤纸、烧杯、玻璃棒、250mL容量瓶、胶头滴管。
(2)配制0.50mol/L NaCl溶液250mL,需要氯化钠的质量m="0.25L×0.50mol/L×58.5" g/mol=7.3g。
(3)根据上述计算,需要称取7.3g氯化钠固体,需要用5g砝码和2.3g游码,则游码的正确位置为![]() 。
。
(5)依据配制溶液的原理,必须将称取的溶质全部转移到容量瓶,而烧杯和玻璃棒上沾有溶质,所以需要洗涤烧杯和玻璃棒2~3次是为了保证溶质全部转移到容量瓶中。
(8)A.转移时有少量溶液溅出,导致溶质减少,所配溶液浓度偏低;B.容量瓶用蒸馏水洗净后未干燥对测定结果无影响;C.定容时俯视读取刻度,导致水加少了,所配溶液浓度偏高,D.定容时液面超过了刻度线,水加多了,导致所配溶液浓度偏低,E.称量NaCl时用了生锈的砝码,溶质增多,导致所配溶液浓度偏高,答案选CE。
(9)必须在烧杯中溶解固体,①错误;定容时,玻璃棒的末端应该抵在刻度线的下方,③错误;定容时平视刻度线,⑤错误;答案为①③⑤。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案