题目内容
将5.5 g铁铝混合物粉末加入900mL 1.00 mol/L HNO3溶液中,充分反应后,得a L(标准状况)NO气体。
(1)HNO3是否过量___________。
(2)若a=3.36L(标准状况),则混合物中铝的质量分数为_________%。
(3)若a=3.36L(标准状况),往反应后的溶液中加入___________ mL 1.000 mol/L NaOH溶液时生成的沉淀量最大,还要加________ mL 1.000 mol/L NaOH溶液才能使沉淀的量保持不变。
(1)是
(2)49.09%
(3)750 100
解析试题分析:(1)铁与等质量的铝与硝酸反应,铝消耗硝酸多,若5.5g固体全部是铝,则Al~4HNO3,n(Al)=5.5/27mol,n(HNO3)=0.9mol>4n(Al),所以硝酸过量;
(2)若a=3.36L,NO的物质的量为0.15mol,设铝的物质的量为x,根据得失电子守恒,有3x+(5.5-27x)/56×3=0.15×3,解得x=0.1mol,所以混合物中铝的质量分数为0.1mol×27g/mol/5.5g×100%=49.09%
(3)沉淀量最大时,溶液恰为硝酸钠的溶液,所以n(NaNO3)= n(HNO3)-n(NO)=0.9mol-0.15mol=0.75mol,根据钠元素守恒,需1.000 mol/L NaOH溶液的体积是750mL;由(2)知生成氢氧化铝的物质的量为0.1mol,当氢氧化铝全部溶解时沉淀量不再改变。根据Al(OH)3~OH-所以还需0.1mol氢氧化钠,其体积为100mL。
考点:考查混合物的计算,得失电子守恒、元素守恒规律的应用

 中考解读考点精练系列答案
中考解读考点精练系列答案利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g) 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g) 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
则ΔH 1= (用含ΔH 2和ΔH 3的代数式表示)。
(2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如图。请回答:
①从反应开始至a点时的反应速率为v(CO)= ,b点时化学平衡常数Kb= 。
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线。
③下列说法正确的是 。(填字母序号)
| A.容器内气体密度不变,表明反应达到平衡状态 |
| B.两种温度下,c点时体系中混合气体的平均相对分子质量相等 |
| C.增加I2O5的投料量有利于提高CO的转化率 |
| D.b点和d点的化学平衡常数:Kb<Kd |
Ⅰ.在一体积为10 L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,CO和H2O浓度变化如图所示:
CO2(g)+H2(g) ΔH<0,CO和H2O浓度变化如图所示:
(1)0~4 min的平均反应速率v(CO)=________mol/(L·min),反应在第5 min时的平衡常数K=________。
t℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0. 200 | 0. 300 | 0 | 0 |
| 2 | 0. 138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0. 116 | 0. 216 | 0. 084 | |
| 6 | 0. 096 | 0. 266 | 0. 104 | |
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表所示:
①表中3~4 min之间反应处于________状态;c1数值________(填“>”“=”或“<”)0.08 mol/L。
②反应在4~5 min间,平衡向逆反应方向移动,可能的原因是________(填标号,下同),表中5~6 min之间数值发生变化,可能的原因是________。
A.增加水蒸气B.降低温度C.使用催化剂D.增加氢气浓度
Ⅱ.在热的稀硫酸中溶解了11.4 g硫酸亚铁固体,当加入50 mL 0.5 mol/L的KNO3溶液后,使其中的Fe2+全部转化成Fe3+、KNO3也完全反应并放出NxOy气体。
(3)推算出x=________,y=________。
(4)写出该反应的化学方程式:________________(x、y用具体数值表示)。
(5)反应中氧化产物是________。
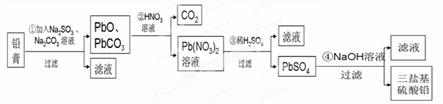

 R ②R+H2O→NaOH+Y ③Q+NaOH→V+W+H2O ④X
R ②R+H2O→NaOH+Y ③Q+NaOH→V+W+H2O ④X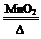 W+Y
W+Y Q+Z+H2O。其中M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
Q+Z+H2O。其中M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
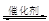 2CO2(g) +N2(g),在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g) +N2(g),在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。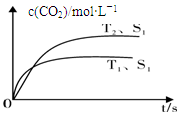
 Fe2+(aq)+S2-(aq),Ksp=c(Fe2+)·c(S2-),常温下Ksp=1.0×10-16。又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:[c(H+)]2·c(S2-)=1.0×10-22,为了使溶液中c(Fe2+)达到1 mol/L,现将适量FeS投入其饱和溶液中,应调节溶液中的pH为 。
Fe2+(aq)+S2-(aq),Ksp=c(Fe2+)·c(S2-),常温下Ksp=1.0×10-16。又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:[c(H+)]2·c(S2-)=1.0×10-22,为了使溶液中c(Fe2+)达到1 mol/L,现将适量FeS投入其饱和溶液中,应调节溶液中的pH为 。

 则
则