题目内容
Ⅰ.在一体积为10 L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,CO和H2O浓度变化如图所示:
CO2(g)+H2(g) ΔH<0,CO和H2O浓度变化如图所示:
(1)0~4 min的平均反应速率v(CO)=________mol/(L·min),反应在第5 min时的平衡常数K=________。
t℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0. 200 | 0. 300 | 0 | 0 |
| 2 | 0. 138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0. 116 | 0. 216 | 0. 084 | |
| 6 | 0. 096 | 0. 266 | 0. 104 | |
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表所示:
①表中3~4 min之间反应处于________状态;c1数值________(填“>”“=”或“<”)0.08 mol/L。
②反应在4~5 min间,平衡向逆反应方向移动,可能的原因是________(填标号,下同),表中5~6 min之间数值发生变化,可能的原因是________。
A.增加水蒸气B.降低温度C.使用催化剂D.增加氢气浓度
Ⅱ.在热的稀硫酸中溶解了11.4 g硫酸亚铁固体,当加入50 mL 0.5 mol/L的KNO3溶液后,使其中的Fe2+全部转化成Fe3+、KNO3也完全反应并放出NxOy气体。
(3)推算出x=________,y=________。
(4)写出该反应的化学方程式:________________(x、y用具体数值表示)。
(5)反应中氧化产物是________。
(1)0.03 1
(2)①平衡 > ②D A
(3)1 1
(4)6FeSO4+2KNO3+4H2SO4=K2SO4+3Fe2(SO4)3+2NO↑+4H2O
(5)Fe2(SO4)3
解析

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目

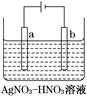
 。
。 Cr2O72-(橙色)+H2O。
Cr2O72-(橙色)+H2O。 Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):____________________________________________________________________________。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol·L-1时,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):____________________________________________________________________________。

 CeO2·8OH + 8_____↑;CeO2·8OH
CeO2·8OH + 8_____↑;CeO2·8OH