题目内容
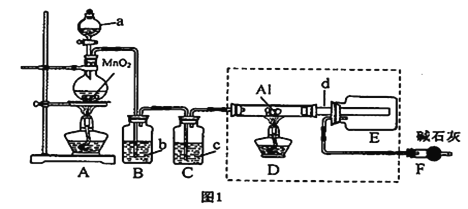
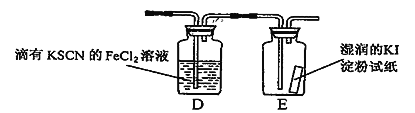
【题目】某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为( )

A. 1∶1∶4
B. 1∶3∶1
C. 3∶3∶8
D. 1∶1∶1
【答案】A
【解析】试题分析:氧化性强弱顺序:HNO3>Fe3+>Cu2+,0~1时发生Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,消耗1molFe的同时消耗4mol硝酸,生成1molFe3+,1~2时发生Fe+2Fe3+=3Fe2+,消耗1molFe同时消耗2molFe3+,因此原溶液中Fe3+的物质的量为1mol,2~3时发生Fe+Cu2+=Fe2++Cu,消耗1molFe的同时消耗1molCu2+,则原溶液中有1 molCu2+,溶液的体积相同,浓度之比等于物质的量之比为:1:1:4,故选项A正确。

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目