题目内容
【题目】合成气经压缩升温后进入10m3的甲醇合成塔中,在催化剂的作用下进行甲醇合成,主要反应是:2H2(g) + CO(g)![]() CH3OH(g)+181.6kJ。已知:某温度下(设温度为T1℃)此反应的平衡常数为160。
CH3OH(g)+181.6kJ。已知:某温度下(设温度为T1℃)此反应的平衡常数为160。
(1)此温度下,在密闭容器中加入一定量的CO和H2,反应到某时刻测得各组分的浓度如表:
物质 | H2 | CO | CH3OH |
浓度/(mol/L) | 0.2 | 0.1 | 0.4 |
比较此时正、逆反应速率的大小:v正_______v逆 (填“>”、“<”或“=”);若加入与上述同样多的CO和H2,在T2℃条件下反应,10 min后达平衡时c(H2)=0.4mol/L,则该时间内反应速率v(CH3OH)=_______ mol/(L·min);
(2)在一定条件的密闭恒容的容器中,下列式子或文字描述能表示上述反应达到化学平衡状态的是_______(选填序号);
a.2v逆(CO) = v正(H2)
b.c(CO): c(H2):c(CH3OH) =1:2:1
c.混合气体的平均式量保持不变
d.混合气体的密度保持不变
(3)上述反应达到平衡后,下列说法正确的是_______(选填序号);
a.其他条件不变,增大压强,平衡常数K﹤160
b.其他条件不变,温度升高,平衡常数K会减小
c.其他条件不变,若同比例地增加CO和H2的量平衡不会发生移动
d.其他条件不变,增大甲醇的物质的量,正反应速率也会随之逐渐增大
(4)寻找合适的催化剂来改善上述合成甲醇的条件一直是研究课题。现分别对X、Y、Z三种催化剂进行如下实验(其他条件均相同):
①X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂并简述理由____。
【答案】> 0.03 ac bd Z,温度要求低,反应速率快
【解析】
(1)根据浓度商与K的大小比较判断;先根据表中数据计算H2的起始浓度,然后计算v(H2),根据速率之比等于化学计量数之比计算;
(2)依据反应特征和平衡标志分析,正逆反应速率相同,各组分含量保持不变分析;
(3)a.其他条件不变,增大压强,平衡常数不变;
b.其他条件不变,温度升高,反应是放热反应,平衡逆向进行,平衡常数K会减小;
c.其他条件不变,若同比例地增加CO和H2的量,相当于增大压强,平衡正向进行;
d.其他条件不变,增大甲醇的物质的量,平衡逆向进行,正逆反应速率也会随之逐渐增大;
(4)根据题给温度和催化剂对反应速率的影响对比分析。
(1)某时刻的Qz=![]() =
=![]() =100<160,反应正向进行,v正>v逆;某时刻CH3OH的浓度为0.4mol/L,则H2的起始浓度为0.2mol/L+0.4mol/L×2=1mol/L,在T2℃反应10min时间内v(H2)=
=100<160,反应正向进行,v正>v逆;某时刻CH3OH的浓度为0.4mol/L,则H2的起始浓度为0.2mol/L+0.4mol/L×2=1mol/L,在T2℃反应10min时间内v(H2)=![]() =0.06mol/(L·min),则v(CH3OH)=
=0.06mol/(L·min),则v(CH3OH)=![]() v(H2)=0.03mol/(L·min),故答案为:>,0.03mol/(L·min);
v(H2)=0.03mol/(L·min),故答案为:>,0.03mol/(L·min);
(2)2H2(g)+CO(g)CH3OH(g)+181.6kJ,反应是气体体积减小的放热反应;
a. 反应速率之比等于化学方程式计量数之比,2v逆(CO)=v正(H2),说明一氧化碳正逆反应速率相同,说明反应达到平衡状态,故a正确;
b. c(CO): c(H2):c(CH3OH)=1:2:1,只能说明浓度比等于反应比,和起始量变化量有关,不能说明反应达到平衡,故b错误;
c.反应前后气体物质的量减小,质量不变,混合气体的平均式量保持不变,说明反应达到平衡状态,故c正确;
d.反应前后气体质量和体积不变,混合气体的密度始终保持不变,不能说明反应达到平衡状态,故d错误;故答案为:ac;
(3)a.其他条件不变,增大压强,平衡常数不变,故a错误;
b.其他条件不变,温度升高,反应是放热反应,平衡逆向进行,平衡常数K会减小,故b正确;
c.其他条件不变,若同比例地增加CO和H2的量,相当于增大压强,平衡正向进行,故c错误;
d.其他条件不变,增大甲醇的物质的量,增大生成物浓度,平衡逆向进行,正逆反应速率也会随之逐渐增大,故d正确;故答案为:bd;
(4)因为T1>T2>T3,所以温度越低平衡常数越大,反应物转化率越大,又催化剂同等程度加快反应速率,所以既能在低温下作用又能加快反应速率的催化剂最好选用Z,故答案为:Z,温度要求低,反应速率快。

 出彩同步大试卷系列答案
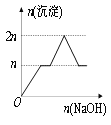
出彩同步大试卷系列答案【题目】含MgCl2、AlCl3均为nmol的混合液,向其中滴加NaOH溶液至过量。有关离子沉淀或沉淀溶解与pH的关系如下表。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是( )
离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
开始沉淀pH | 8.93 | 3.56 | 开始溶解pH | 8.04 |
完全沉淀pH | 10.92 | 4.89 | 完全溶解pH | 12.04 |
A. B.
B.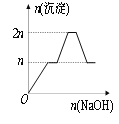
C.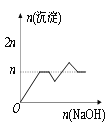 D.
D.