题目内容
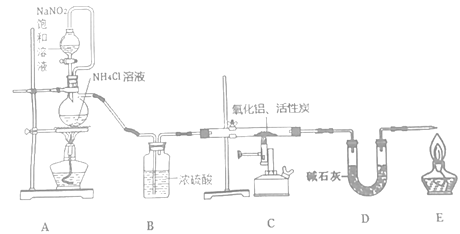
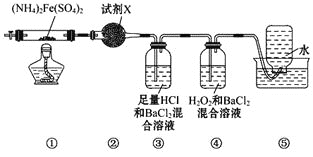
【题目】实验室用如图装置进行硫酸亚铁铵[(NH4)2Fe(SO4)2]的分解反应并确定分解产物成分。已知在500℃时隔绝空气加热分解的固体产物可能有FeO、Fe2O3和Fe3O4,气体产物可能有NH3、N2、H2O、SO3和SO2。下列说法正确的是( )
A.取①中固体残留物与稀硫酸反应并滴加KSCN,溶液变红,则气体产物一定有SO2
B.装置②用于检验分解产物中是否有水蒸气生成,试剂X可以使用无水氯化钙
C.装置③的作用就是检验分解产物中是否有SO3气体生成并除去SO3
D.装置④用于检验分解产物中是否有SO2气体生成,装置⑤用于收集生成的NH3和N2
【答案】A
【解析】
实验室用如图装置进行硫酸亚铁铵[(NH4)2Fe(SO4)2]的分解反应, 分解的固体产物可能有FeO、Fe2O3和Fe3O4,气体产物可能有NH3、N2、H2O、SO3和SO2,②中的试剂应为硫酸铜,用于检验生成的水,③可用于检验SO3并吸收NH3,④用于检验SO2,H2O2可氧化SO2生成H2SO4,⑤用于收集N2,据此分析解答。
A. 如不含Fe2O3,而含有Fe3O4,则加入盐酸可生成氯化铁,滴加KSCN,溶液变红,反应中Fe的化合价升高,若生成N2,N的化合价也升高,则S的化合价降低,则有SO2生成,A项正确;
B. 应用硫酸铜检验水,用无水氯化钙没有明显的现象, B项错误;
C. 装置③中盐酸可吸收氨气,水与三氧化硫反应生成硫酸,可生成硫酸钡沉淀, C项错误;
D. ④用于检验SO2,过氧化氢可氧化SO2生成硫酸,⑤用于收集氮气, D项错误。
答案选A。

练习册系列答案
相关题目