题目内容
恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应3A(g)+2B(g) 2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 、2 mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol·(L·min)-1。N:2 mol C 、y mol D;达平衡时c(A)="0.6" mol·L-1。下列推断的结论中不正确的是
2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 、2 mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol·(L·min)-1。N:2 mol C 、y mol D;达平衡时c(A)="0.6" mol·L-1。下列推断的结论中不正确的是
A.x=2 B.平衡时M中c(A)>0.6 mol/L
C.y≥2 D.M、N达到平衡时容器中各物质浓度相等
B
解析试题分析:解:A从反应开始到平衡,C的速率为0.3mol/(L?min),则△n(C)=0.3mol/(L?min)×2min×2L=1.2mol,物质的量之比等于化学计量数之比,所以2:x=1.2mol:1.2mol,解得x=2,故A正确;B从反应开始到平衡,C的速率为0.3mol/(L?min),所以△c(C)=0.3mol/(L?min)×2min=0.6mol/L,浓度变化量之比等于化学计量数之比,所以△c(A)=3/2△c(C)=3/2×0.6mol/L=0.9mol/L,所以平衡时c(A)=1.5mol/L-0.9mol/L=0.6mol/L,故B不正确;C由B中计算可知M中A的平衡浓度为0.6mol/L,所以M、N是等效平衡,则按化学计量数转化到左边满足n(A)=3mol,n(B)=2mol,恰好转化时y=3mol×2/3=2mol,由于D为固体,故y≥2,故C正确;D由C中分析可知y≥2,故D正确;故选B。
考点:本题考查的是平衡移动的影响因素、等效平衡原理应用。

在一定条件下,向一带活塞的密闭容器中充入2mol NO2,发生下列反应2NO2(g)  N2O4(g) ΔH < 0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推测中正确的是
N2O4(g) ΔH < 0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推测中正确的是
| A.保持压强不变,升高反应温度 |
| B.保持温度和容器体积不变,充入1mol N2(g) |
| C.保持温度和容器体积不变,充入1mol N2O4(g) |
| D.保持温度和压强不变,充入1mol N2O4(g |
在相同温度下,体积均为1 L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应。平衡时有关数据如下(已知2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6 kJ·mol-1)。
2SO3(g)ΔH=-196.6 kJ·mol-1)。
| 容器 | 甲 | 乙 | 丙 | 丁 |
| 起始投料量 | 2 mol SO2+1 mol O2 | 1 mol SO2+0.5 mol O2 | 2 mol SO3 | 2 mol SO2+2 mol O2 |
| 反应放出或吸收的热量(kJ) | a | b | c | d |
| 平衡时c(SO3) (mol·L-1) | e | f | g | h |
下列关系正确的是( )
A.a=c;e=g B.a>2b;e>2f C.a>d;e>h D.c+98.3e>196.6
在一定温度下将各1mol CO和水蒸气放在密闭的容器中反应:
CO(g)+H2O(g) CO2(g)+ H2(g) 达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为
CO2(g)+ H2(g) 达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为
| A.等于0.6mol | B.等于1mol | C.大于0.6mol小于1mol | D.大于1mol |
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s,白)+2HCl(aq)=SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)=SnCl2(aq)+H2(g) ΔH2
③Sn(s,灰) 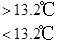 Sn(s,白) ΔH3=+2.1 kJ·mol-1
Sn(s,白) ΔH3=+2.1 kJ·mol-1
下列说法正确的是 ( )
| A.ΔH1>ΔH2 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是放热反应 |
| D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏 |
一定条件下,在容积不变的密闭容器中加入P、Q进行反应P(g)+2Q(g)  3R(g)+S(l),说明该反应已达到平衡的是
3R(g)+S(l),说明该反应已达到平衡的是
| A.反应容器中气体的平均摩尔质量不再改变 |
| B.反应容器中P、Q、R、S四者共存 |
| C.2v正(Q)="3" v逆(R) |
| D.反应容器中压强不随时间变化而变化 |
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为CO(g)+ H2O(g)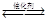 CO2(g) + H2(g) △H<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是
CO2(g) + H2(g) △H<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增加压强 | B.降低温度 | C.增大CO 的浓度 | D.更换催化剂 |
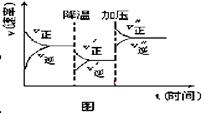
 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断