��Ŀ����
����Ŀ��ʵ������⣺ʵ������Ҫ��ȡһƿ���������������������ͼ������ҩƷ�ɹ�ʹ�ã� 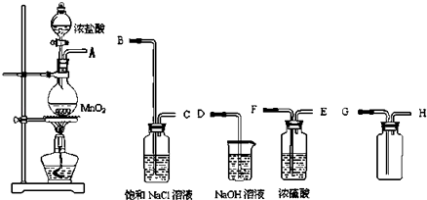
��1��ʵ������ȡ������ԭ����������HCl�����ֵ������� ��
��2������������������ȷ˳���ǣ�����ӿڴ�����ĸ���� �� �� �� �� �� �� ��
��3��������װ���У��ֱ�ʢװ��һЩ��Һ����˵����װ��Һ�����ã�����ʳ��ˮ����������Ũ��������������������Ƶ������� ��
��4��ʢװNaOH��Һ���Լ�ƿ�з����Ļ�ѧ��ӦΪ�� ��
���𰸡�
��1��MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O�����ԡ���ԭ��
MnCl2+Cl2��+2H2O�����ԡ���ԭ��
��2��A��B��C��F��E��G��H��D
��3����ȥ�Ȼ����������壻�������������ն��������
��4��2NaOH+Cl2 =NaCl+NaClO+H2O
���������⣺��1��ʵ�������ö������̺�Ũ���ᷴӦ������������Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O����Ӧ�У�MnԪ�صĻ��ϼ۽��ͣ�ClԪ�صû��ϼ����ߣ���MnO2Ϊ��������HClΪ��ԭ�����ɷ���ʽ��֪�����Ȼ������ȵĻ��ϼ�δ�䣬���ԣ������ڷ�Ӧ�������Ժͻ�ԭ�������ã� ���Դ��ǣ�MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O����Ӧ�У�MnԪ�صĻ��ϼ۽��ͣ�ClԪ�صû��ϼ����ߣ���MnO2Ϊ��������HClΪ��ԭ�����ɷ���ʽ��֪�����Ȼ������ȵĻ��ϼ�δ�䣬���ԣ������ڷ�Ӧ�������Ժͻ�ԭ�������ã� ���Դ��ǣ�MnO2+4HCl��Ũ�� ![]() MnCl2+Cl2��+2H2O�����ԡ���ԭ�ԣ���2��ʵ�����õ�һ��װ���Ʊ�����������ֱ�ͨ��ʢ�б����Ȼ�����Һ��ϴ��ƿ��ʢ��Ũ�����ϴ��ƿ�����Ӹ�����������ſշ��ռ������������ж�������ֱ���ŷŵ������У�Ӧ��ʢ��NaOH��Һ��װ�����գ�
MnCl2+Cl2��+2H2O�����ԡ���ԭ�ԣ���2��ʵ�����õ�һ��װ���Ʊ�����������ֱ�ͨ��ʢ�б����Ȼ�����Һ��ϴ��ƿ��ʢ��Ũ�����ϴ��ƿ�����Ӹ�����������ſշ��ռ������������ж�������ֱ���ŷŵ������У�Ӧ��ʢ��NaOH��Һ��װ�����գ�
���Դ��ǣ�ABCFEGHD����3�������ӷ���������ȡ�������л����Ȼ��������ˮ�������Ȼ��⼫������ˮ������Ҳ������ˮ�����Բ�����ˮ��ȥ�Ȼ������壻������ˮ��Ӧ��������ʹ����ᣬ����ʳ��ˮ�к��������ӣ��������������ܽ⣬���Ա���ʳ��ˮ�������dz�ȥ�Ȼ����������壻Ũ���᳣�������ܸ������ԡ��������壬��ѡŨ����������������������������������Һ���գ�
���Դ��ǣ���ȥ�Ȼ����������壻�������������ն������������4�������ж�����Ⱦ���������Բ���ֱ���ſգ������ܺ��������Ʒ�Ӧ2NaOH+Cl2 =NaCl+NaClO+H2O�����Կ�������������Һ���ն����������
���Դ��ǣ�Cl2+2NaOH=NaCl+NaClO+H2O��
�����㾫��������������ʵ�����Ʒ��ǽ����ĸ�������Ҫ֪��ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O��

 ��������ϵ�д�
��������ϵ�д�