题目内容
新型高效多功能水处理剂Na2FeO4的制备方法可用化学方程式表示为:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法不正确的是( )
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法不正确的是( )
| A、在反应中Na2FeO4只是氧化产物 | ||
B、在反应中有
| ||
| C、2mol FeSO4发生反应时,共有10mol电子转移 | ||
| D、此反应氧化剂为Na2O2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应中Fe元素化合价由+2价变为+6价、过氧化钠中O元素化合价由-1价变为0价和+2价,据此分析解答.
解答:
解:A.该反应中Fe元素化合价由+2价变为+6价、过氧化钠中O元素化合价由-1价变为0价和+2价,所以Na2FeO4和氧气为氧化产物,故A错误;
B.反应中有
的Na2O2作还原剂被氧化,故B正确;
C.2mol FeSO4发生反应时,转移电子的物质的量=2mol×4+1mol×2=10mol,故C正确;
D.该反应中氧化剂只有Na2O2,还原剂为Na2O2和FeSO4,故D正确;
故选A.
B.反应中有
| 1 |
| 6 |
C.2mol FeSO4发生反应时,转移电子的物质的量=2mol×4+1mol×2=10mol,故C正确;
D.该反应中氧化剂只有Na2O2,还原剂为Na2O2和FeSO4,故D正确;
故选A.
点评:本题考查了氧化还原反应,根据元素化合价变化结合基本概念分析解答,注意过氧化钠的作用,会计算过氧化钠中作氧化剂和还原剂的物质的量之比,为易错点.

练习册系列答案
相关题目
观察如图几个装置示意图,有关叙述正确的是( )
A、装置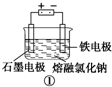 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 |
B、装置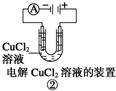 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 |
C、装置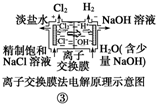 中的离子交换膜只允许阳离子、阴离子和小分子水通过 中的离子交换膜只允许阳离子、阴离子和小分子水通过 |
D、装置 的待镀铁制品应与电源正极相连 的待镀铁制品应与电源正极相连 |
下列关于Fe(OH)3胶体的说法中不正确的是( )
| A、Fe(OH)3胶体与硅酸溶液混合将产生凝聚现象 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极移动 |
| C、液溶胶中Fe(OH)3胶体粒子不停地做布朗运动 |
| D、光线通过Fe(OH)3胶体时会发生丁达尔现象 |
下列电离方程式中正确的是( )
| A、H2SO4=H2++SO42- |
| B、NaHCO3=Na++H++CO32- |
| C、Ca(OH)2=Ca2++2OH- |
| D、CaCl2=Ca+2+2Cl- |
下列关于化石燃料及其加工说法正确的是( )
| A、天然气和沼气的主要成分都是甲烷,二者都是不可再生资源 |
| B、石油分馏和煤千馏都是物理变化,前者可得到汽油、煤油等,后者主要得到焦炭、煤焦油、粗氨水和焦炉气 |
| C、石油裂化主要是为了提高轻质油的产量,尤其是汽油的产量 |
| D、煤的液化指的是把煤加热到熔点以上使其变成液体 |
下列说法正确的是( )
| A、强电解质溶液的导电能力比弱电解质强 |
| B、难溶盐如:BaSO4、CaCO3、AgCl等是弱电解质,易溶性盐如:醋酸铵是强电解质 |
| C、在水溶液中是否完全电离是判断强弱电解质的依据 |
| D、二氧化硫溶于水可以导电,所以二氧化硫是电解质 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、32g硫在足量的O2中燃烧生成的SO3分子数等于NA |
| B、1mol Cl2与足量的NaOH溶液反应,转移的电子数为2NA |
| C、常温常压下,25g甲醛所含电子数为10NA |
| D、在标准状态下,68g H2O2中含有的6mol共价键 |
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A、该电池工作时电能转化为化学能 |
| B、该电池中电极a是正极 |
| C、该电池的总反应:2H2+O2═2H2O |
| D、外电路中电子由电极b通过导线流向电极a |
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、T℃时,1 L pH=6纯水中,约含6.02×1017个OH- |
| B、6.8g熔融的KHSO4中含有6.02×1022个阳离子 |
| C、Na2O2与H2O反应,生成常温常压下16g O2,反应中转移电子数为2NA |
| D、用含有0.1mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒个数等于0.1NA |