题目内容
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 将0.1molCl2通入一定量水中,HClO、Cl-、ClO-粒子数之和为0.2NA
B. 12gNaHSO4固体中含阳离子数为0.1NA
C. 将1molFe(OH)3加入到含3molHI的溶液完全反应后,溶液中所含I- 的数目为3NA
D. 已知合成氨反应N2(g)+3H2(g) ![]() 2NH3(g) △H= —92.4 kJ·mol-1,当该反应生成NA个NH3分子时,反应放出的热量大于46.2kJ
2NH3(g) △H= —92.4 kJ·mol-1,当该反应生成NA个NH3分子时,反应放出的热量大于46.2kJ
【答案】B
【解析】A. 氯水中存在平衡关系:Cl2+H2O![]() H++Cl-+HClO,将0.1molCl2通入一定量水中,HClO、Cl-、ClO-粒子数之和小于0.2NA,A错误;B. NaHSO4是由钠离子和硫酸氢根离子构成的离子化合物,12gNaHSO4是0.1mol,固体中含阳离子数为0.1NA,B正确;C. 将1molFe(OH)3加入到含3molHI的溶液中发生氧化还原反应生成亚铁离子和碘单质,完全反应后碘离子过量,所以根据电子得失守恒可知溶液中所含I- 的数目为2NA,C错误;D. 已知合成氨反应N2(g)+3H2(g)
H++Cl-+HClO,将0.1molCl2通入一定量水中,HClO、Cl-、ClO-粒子数之和小于0.2NA,A错误;B. NaHSO4是由钠离子和硫酸氢根离子构成的离子化合物,12gNaHSO4是0.1mol,固体中含阳离子数为0.1NA,B正确;C. 将1molFe(OH)3加入到含3molHI的溶液中发生氧化还原反应生成亚铁离子和碘单质,完全反应后碘离子过量,所以根据电子得失守恒可知溶液中所含I- 的数目为2NA,C错误;D. 已知合成氨反应N2(g)+3H2(g)![]() 2NH3(g) △H= —92.4 kJ·mol-1,当该反应生成NA个NH3分子即1mol氨气时,反应放出的热量为92.4 kJ·mol-1×0.5mol=46.2kJ,D错误,答案选B。
2NH3(g) △H= —92.4 kJ·mol-1,当该反应生成NA个NH3分子即1mol氨气时,反应放出的热量为92.4 kJ·mol-1×0.5mol=46.2kJ,D错误,答案选B。

 阅读快车系列答案
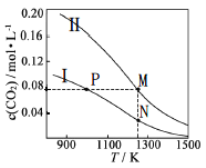
阅读快车系列答案【题目】两个容积均为10L的密闭容器Ⅰ和Ⅱ中发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),起始物质的量见下表。实验测得两容器不同温度下达到平衡时CO2的物质的量浓度如下图所示,下列说法错误的是
N2(g)+2CO2(g),起始物质的量见下表。实验测得两容器不同温度下达到平衡时CO2的物质的量浓度如下图所示,下列说法错误的是
容器 | 起始物质的量 | ||
NO | CO | ||
Ⅰ | 1mol | 0.5mol | |
Ⅱ | 2mol | 1mol | |
A. 反应N2(g)+2CO2(g)![]() 2NO(g)+2CO(g)的ΔH<0,ΔS>0
2NO(g)+2CO(g)的ΔH<0,ΔS>0
B. P点的速率比M点慢
C. M、N两点容器内的压强: P(M) <2P(N)
D. N点的平衡常数为44.4