题目内容
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.Na2S2O3与H2SO4溶液混合产生22.4 L气体时转移电子数为2NA
B.标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为9NA
C.常温下,1 L 0.5 mol/L CH3COONH4溶液的pH=7,则溶液中CH3COO-与NH4+的数目均为0.5NA
D.50g质量分数为46%的乙醇溶液与足量的钠反应,放出H2的分子数目为0.25NA
【答案】B
【解析】
A.未指明气体的状态,无法确定22.4L气体的物质的量是1mol,则反应中转移电子的数目不一定是2NA,故A错误;
B.环丙烷和丙烯分子中均含有9个共用电子对,则标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为![]() ×9NA=9NA,故B正确;
×9NA=9NA,故B正确;
C.CH3COONH4为弱酸弱碱盐,醋酸根离子和铵根离子均会水解,因此1L溶液中CH3COO-与NH4+的数目均小于0.5NA,故C错误;
D.Na与50g质量分数为46%的乙醇溶液反应时,钠先和水反应,后再和乙醇反应;50g46%的乙醇溶液中含有的乙醇的质量为23g,物质的量为0.5mol,故和钠反应生成0.25mol氢气;而水的质量为27g,物质的量为1.5mol,故和钠反应生成0.75mol氢气,故共生成1mol氢气即NA个氢气分子,故D错误;
故答案为B。

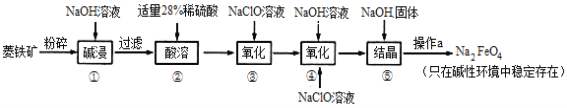
【题目】某地菱锰矿的主要成分为MnCO3,还含有少量的FeCO3、CaCO3、Al2O3等杂质。工业上以菱锰矿为原料制备高纯度碳酸锰的流程如图所示:
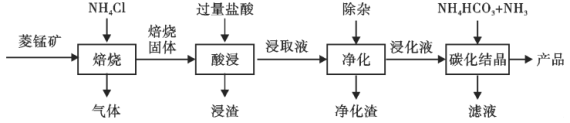
已知:MnCO3+2NH4Cl=MnCl2+CO2↑+2NH3↑+H2O.
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 |
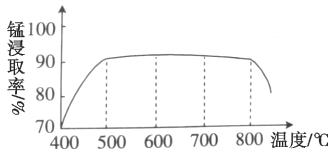
(1)焙烧时温度对锰浸取率的影响如图。焙烧时适宜的温度为___________左右;800℃以上锰的浸取率偏低,可能的原因是___________。
(2)净化包含三步:①加入少量MnO2,添加少量MnO2的作用是____________。发生反应的离子方程式为___________。
②加氨水调pH,溶液的pH范围应调节为___________~8.1之间。生成的沉淀主要是___________。
③加入MnF2,沉淀除去Ca2+,若溶液酸度过高,Ca2+沉淀不完全,原因是___________。
(3)碳化结晶中生成MnCO3的离子方程式为____________。