题目内容
9.化学风化是地壳表面岩石和矿物在大气和水的作用下发生的化学成分和矿物组成的变化,形成土壤和次生岩石的过程,主要有:(1)溶解作用:岩石中的碳酸钙溶解于含有CO2的水中,该过程在低温下溶解较快的原因是低温下,水中二氧化碳浓度大,反应速率加快;
(2)水解作用:岩石中的硅酸盐可发生水解使矿物风化,如正长石[KAlSi3O8]在湿热气候条件下,水解形成高岭石[Al2Si2O5(OH)x],同时形成H4SiO4及另一种含钾化合物,则x=4,含钾化合物的化学式:KHCO3;
(3)氧化作用:岩石中的硫化物易被氧化.如黄铁矿[FeS2]在潮湿空气中氧化形成褐铁矿[Fe2O3•nH2O]和H2SO4,写出化学方程式:4FeS2+15O2+(8+n)H2O=2Fe2O3•nH2O+8H2SO4.
分析 (1)发生反应:CaCO3+CO2+H2O=Ca(HCO3)2,水中二氧化碳浓度越大,反应速率越快;
(2)根据化合价代数和为0计算x的值;
KAlSi3O8与H2O和CO2同时作用的过程,生成高岭土[Al2Si2O5(OH)4],H4SiO4,此反应的离子方程式是:2KAlSi3O8+11H2O+2CO2=2K++2HCO3-+4H4SiO4+Al2Si2O5(OH)4;
(3)由题目信息可知,FeS2与氧气、水反应生成Fe2O3•nH2O和H2SO4.
解答 解:(1)发生反应:CaCO3+CO2+H2O=Ca(HCO3)2,低温下,水中二氧化碳浓度大,反应速率加快,
故答案为:低温下,水中二氧化碳浓度大,反应速率加快;
(2)根据化合价代数和为0,则3×2+4×2+(-2)×5+(-1)×x=0,解得x=4;
KAlSi3O8与H2O和CO2同时作用的过程,生成高岭土[Al2Si2O5(OH)4],H4SiO4,此反应的离子方程式是:2KAlSi3O8+11H2O+2CO2=2K++2HCO3-+4H4SiO4+Al2Si2O5(OH)4,含钾化合物的化学式:KHCO3,
故答案为:4;KHCO3;
(3)由题目信息可知,FeS2与氧气、水反应生成Fe2O3•nH2O和H2SO4,反应方程式为:4FeS2+15O2+(8+n)H2O=2Fe2O3•nH2O+8H2SO4,
故答案为:4FeS2+15O2+(8+n)H2O=2Fe2O3•nH2O+8H2SO4.
点评 本题以岩石形成土壤为载体,考查化学反应速率影响因素、硅酸盐、化学方程式书写等,(2)为易错点、难点,是对学生综合能力的考查,难度中等.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
19.下列递变规律不正确的是( )
| A. | Na、Mg、Al还原性依次减弱 | B. | I2、Br2、Cl2氧化性依次增强 | ||
| C. | F、Cl、Br氢化物的沸点依次升高 | D. | P、S、Cl最高正价依次升高 |
20.已知25℃、101kPa条件下,H2、CO、CH4的燃烧分别为286kJ•mol-1、283kJ•mol-1、890kJ•mol-1,若将a mol H2、CO、CH4的混合气体完全燃烧,生成气态CO2和液态H2O,且n(CO2)=n(H2O),则放出的热量(Q)可能为( )
| A. | 284.5a kJ | B. | 586.5a kJ | C. | 555a kJ | D. | 598a kJ |
17.下面三种方法都可以制得氯气.
①MnO2+4HCl(浓)═MnCl2+Cl2+2H2O
②2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2+8H2O
③4HCl(浓)+O2$\frac{\underline{催化剂}}{△}$2H2O+Cl2
这三种氧化剂的氧化性由强到弱的顺序是( )
①MnO2+4HCl(浓)═MnCl2+Cl2+2H2O
②2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2+8H2O
③4HCl(浓)+O2$\frac{\underline{催化剂}}{△}$2H2O+Cl2
这三种氧化剂的氧化性由强到弱的顺序是( )
| A. | O2>MnO2>KMnO4 | B. | KMnO4>MnO2>O2 | C. | MnO2>KMnO4>O2 | D. | O2>MnO2>KMnO4 |
4.不加其他试剂就无法鉴别的一组无色溶液是( )
| A. | NH4NO3、Na2SO4、CuSO4、MgCl2 | B. | MgCl2、BaCl2、NaOH、H2SO4 | ||
| C. | NaBr、AgNO3、HCl、KI | D. | NaNO3、BaCl2、Na2CO3、H2SO4 |
14.下列关于微粒之间作用力的说法正确的是( )
| A. | 在分子中,化学键可能只有π键,而没有σ 键 | |
| B. | 不同元素组成的多原子分子里的化学键一定都是极性键 | |
| C. | 实验测得NO2和CH3COOH 的摩尔质量均比理论值大,可能原因是在实验条件下这两种分子均能发生“双聚”,这种分子“双聚”的作用力是相同类型的作用力 | |
| D. | 原子晶体的熔点一定比分子晶体高,原因之一是共价键是一种比分子间作用力更为强烈的相互作用 |
5.现有一种烃可以表示为 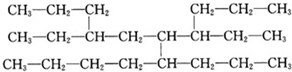 命名该化合物时,应认定它的主链上的碳原子数目为( )
命名该化合物时,应认定它的主链上的碳原子数目为( )
 命名该化合物时,应认定它的主链上的碳原子数目为( )
命名该化合物时,应认定它的主链上的碳原子数目为( )| A. | 9 | B. | 10 | C. | 11 | D. | 12 |
2.下列反应的离子方程式正确的是( )
| A. | 向AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2OA1O2═+4NH4++2H2O | |
| B. | 少量金属钠加到冷水中:Na+2H2O═Na++OH-+H2↑ | |
| C. | 酸性条件下,KIO3溶液与KI溶液反应:IO3-+5I-+3H2O═3I2+6OH- | |
| D. | 浓盐酸与铁屑反应:Fe+2H+═Fe2++H2↑ |