题目内容
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是( )
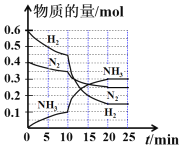
A.一定条件下,3molH2和1molN2充分反应后,可得2NA个NH3分子
B.室温下,1LpH=1的HCl溶液中,由水电离的H+数目为0.1NA
C.0.1mol金属Na在空气中完全氧化生成Na2O和Na2O2,转移的电子数为0.1NA
D.1mol/L的NaCN溶液中含CN-和HCN的数目之和为NA
【答案】C
【解析】
A. 合成氨的反应N2+3H22NH3为可逆反应,不能进行到底,得到的NH3分子小于2NA,A项错误;
B. 室温下,1LpH=1的HCl溶液中,氢离子浓度为0.1mol/L,氢氧根是水电离的,![]() ,水电离的H+的浓度等于水电离的氢氧根的浓度,则水电离的H+浓度为:c(H+)水=10-13mol/L,水电离的H+数目为10-13NA,B项错误;
,水电离的H+的浓度等于水电离的氢氧根的浓度,则水电离的H+浓度为:c(H+)水=10-13mol/L,水电离的H+数目为10-13NA,B项错误;
C. 0.1mol金属Na在空气中完全氧化生成Na2O和Na2O2,Na的化合价都是升高为+1价,所以转移的电子数为0.1NA,C项正确;
D. 缺少溶液的体积,无法计算CN-和HCN的物质的量之和,D项错误;
答案选C。

 寒假学与练系列答案
寒假学与练系列答案【题目】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分。
H | He | ||||||
Li | Be | B | C | N | O | F | Ne |
Na | Mg | Al | Si | P | S | Cl | Ar |
请回答下列问题。
(1)非金属性最强的元素名称为___________,它位于元素周期表中的位置___________。
(2)硅元素的原子结构示意图是____________,其最高价氧化物是____________(填“酸性”或“碱性”)氧化物。
(3)硼酸(H3BO3)的酸性_________(填“>” 或“<”)碳酸(H2CO3)的酸性,说明你判断的理由:__________________________。
(4)NH3的电子式为________________,它属于____________(填“离子”或“共价”)化合物。NH3的还原性_________(填“>” 或“<”)PH3的还原性。
(5)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式______________。