题目内容
【题目】25℃时,向Na2CO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。已知:lgX=lg![]() 或lg
或lg![]() ,下列叙述正确的是( )
,下列叙述正确的是( )
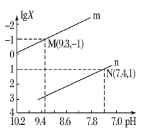
A.曲线m表示pH与lg![]() 的变化关系
的变化关系
B.当溶液呈中性时,c(Na+)=c(HCO3-)+2c(CO32-)
C.Ka1(H2CO3)=1.0×10-7.4
D.25℃时,CO32-+H2OHCO3-+OH-的水解常数为1.0×10-3.7
【答案】D
【解析】
A.溶液的pH越小,CO32-已转化为HCO3- 和H2CO3,HCO3-和![]() 的浓度越大,m曲线代表
的浓度越大,m曲线代表 ,故A错误;
,故A错误;
B.当溶液为中性时,溶液中溶质为氯化钠、碳酸氢钠和碳酸,溶液中电荷守恒为![]() ,则
,则![]() ,故B错误;
,故B错误;
C.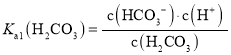 ,在N点lg
,在N点lg![]() =10,N点的
=10,N点的![]() ,则
,则![]() ,所以
,所以![]() ,故C错误;
,故C错误;
D.m曲线代表 pH=-1,
pH=-1,![]() lg
lg![]() .
. ,
,![]() 时,
时,![]() 的水解常数为
的水解常数为![]() ,故D正确;
,故D正确;
答案选D。

练习册系列答案
相关题目
【题目】一定温度下,向2.0L恒容密闭容器中充入2molSO2和1molO2,发生反应为:2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
2SO3(g)。经过一段时间后达到平衡,反应过程中测定的部分数据见下表:下列说法正确的是( )
t/s | 0 | 2 | 4 | 6 | 8 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
A.反应在前2 s的平均速率υ(O2)=0.4 mol·L1·s1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3,达平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2) 增大