题目内容
下列说法正确的是( )
| A、氯化钠熔化或氯化氢溶于水时都要破坏化学键 |
| B、常温常压下,18g D2O含有6.02×1024个电子 |
| C、标准状况下,11.2L SO3所含3.01×1023个分子 |
| D、离子化合物中可能含有共价键,共价化合物中一定不含有离子键 |
考点:不同晶体的结构微粒及微粒间作用力的区别,阿伏加德罗常数,质量数与质子数、中子数之间的相互关系,化学键
专题:化学键与晶体结构
分析:A.氯化钠熔化或氯化氢溶于水都电离出阴阳离子;
B.1个D2O分子中含有10个电子,18g D2O的物质的量=
=0.9mol,据此计算电子总数;
C.标况下,三氧化硫是固体,气体摩尔体积对其不适用;
D.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物.
B.1个D2O分子中含有10个电子,18g D2O的物质的量=
| 18g |
| 20g/mol |
C.标况下,三氧化硫是固体,气体摩尔体积对其不适用;
D.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物.
解答:
解:A.氯化钠熔化或氯化氢溶于水都电离出阴阳离子,所以都要破坏化学键,故A正确;
B.1个D2O分子中含有10个电子,18g D2O的物质的量=
=0.9mol,则电子总数为0.9×6.02×1024个电子,故B错误;
C.标况下,三氧化硫是固体,气体摩尔体积对其不适用,无法计算三氧化硫的物质的量,导致无法计算三氧化硫的分子数,故C错误;
D.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,如KOH,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,故D正确;
故选AD.
B.1个D2O分子中含有10个电子,18g D2O的物质的量=
| 18g |
| 20g/mol |
C.标况下,三氧化硫是固体,气体摩尔体积对其不适用,无法计算三氧化硫的物质的量,导致无法计算三氧化硫的分子数,故C错误;
D.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,如KOH,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,故D正确;
故选AD.
点评:本题考查了物质结构、化学键和化合物的关系、物质的量的计算等知识点,注意B中重水的摩尔质量、C中气体摩尔体积的适用范围及适用条件,这些都是易错点.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
在V mL Al2(SO4)3溶液中含有Al3+m g,取
mL该溶液用水稀释至4V mL,则SO42-物质的量浓度为( )
| V |
| 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
下列化学反应属于加成反应的是( )
| A、油脂的皂化反应 |
| B、苯与浓硝酸、浓硫酸混合反应 |
| C、在一定条件下,苯与氢气的反应 |
| D、乙烯通入溴的四氯化碳溶液中的反应 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、1mol Cl2与足量Fe反应转移电子数一定为3NA |
| B、标准状况下,22.4L NH3中含有共价键的数目为NA |
| C、1.0L 1mol?L-1的硅酸钠水溶液中含有的氧原子数为3NA |
| D、4.6g Na完全转化成氧化钠和过氧化钠的混合物,混合物中阴离子总数为0.1NA |
下列各组物质按单质、电解质、混合物的顺序排列正确的是( )
| A、空气、熟石灰、盐酸 |
| B、液氯、烧碱、漂白粉 |
| C、石英、二氧化硫、硫酸 |
| D、青铜、纯碱、水玻璃 |
除去下列物质中的杂质,所用试剂和方法不正确的是( )
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | KCl溶液 | I2 | CCl4,萃取分液 |
| B | CO2 | HCl | 饱和NaHCO3溶液,洗气 |
| C | FeCl3溶液 | FeCl2 | 过量还原铁粉,过滤 |
| D | Mg粉 | Al粉 | 足量NaOH溶液,过滤 |
| A、A | B、B | C、C | D、D |
X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味).X、Y、Z 三种元素形成化合物乙.下列说法不正确的是( )
| A、原子半径:W>Y>Z>M>X |
| B、X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM |
| C、W与Z两元素形成的化合物是原子晶体 |
| D、化合物乙中一定只有共价键 |
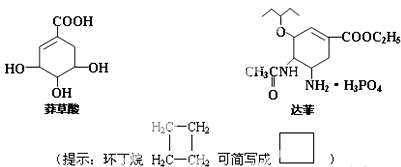
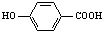 ),其反应类型为:
),其反应类型为: