题目内容
【题目】反应H2(g)+I2(g)![]() 2HI(g)为放热反应,若在恒容绝热的容器中发生,下列选项表明已达平衡状态的是( )
2HI(g)为放热反应,若在恒容绝热的容器中发生,下列选项表明已达平衡状态的是( )
A.气体的总物质的量不再变化
B.容器内的压强不再变化
C.相同时间内,断开H-H键的数目和生成H—I键的数目相等
D.容器内气体的浓度c(H2):c(I2):c(HI)=1:1:2
【答案】B
【解析】
可逆反应,若正反应速率等于逆反应速率,或各物质的浓度、物质的量分数等保持不变,则表明反应一定已达平衡状态,据此分析作答。
A.根据反应可知,该反应前后气体的总物质的量始终不发生改变,因此气体的总物质的量不再变化不能说明反应达到平衡,A不符合题意;
B.在恒容绝热的容器中,容器内的压强为变量,当容器内的压强不再发生改变时,反应达到平衡,B符合题意;
C.相同时间内,断开H—H键的数目和生成H—I键的数目相等,表示的都是正反应,不能判断反应是否达到平衡,C不符合题意;
D.容器内气体的浓度c(H2):c(I2):c(HI)=1:1:2,无法判断各组分的浓度是否发生变化,无法说明反应达到平衡状态,D不符合题意;
答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展做出重要贡献的科学家。利用废旧二次电池[主要成分为Ni(OH)2、Fe2O3、MnO2、碳粉、铝箔等]合成电池级Ni(OH)2的工艺流程如下:
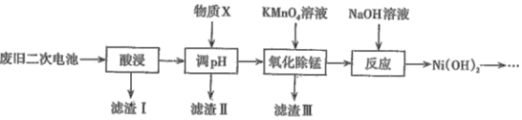
已知:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | Mn(OH)2 |
Ksp(室温下) | 4.0×10-38 | 1.0×10-33 | 1.6×10-14 | 2.0×10-13 |
(1)①已知“酸浸”后滤液中含有:Ni2+、Al3+、Fe3+、Mn2+,调节溶液的pH约为5,其目的是__;以下最适合作为物质X的是____(填字母)。
A.双氧水 B.氨水 C.盐酸 D.NiO
②若滤液中Ni2+的浓度为2molL-1,列式计算判断此时滤渣Ⅱ中是否有Ni(OH)2沉淀:___ 。
(2)滤渣Ⅲ的主要成分是____,“氧化除锰”过程发生反应的离子方程式为______。
(3)用Ni(OH)2和LiOH在空气中混合加热至700℃~800℃可制得LiNiO2(镍酸锂),该反应的化学方程式为___________。
(4)镍酸锂是一种有较好前景的锂离子电池正极材料。该电池在充放电过程中,发生LiNiO2和Li1-xNiO2之间的转化,充电时LiNiO2在_______(填“阴”或“阳“)极发生反应,该电极的电极反应式为_____。