题目内容
【题目】吊白块(NaHSO2·HCHO·2H2O)可用作印染工业的还原剂、橡胶合成及制糖工业中的漂白剂。以SO2、纯碱、Zn及甲醛为原料生产吊白块及氧化锌的工艺流程如图:

已知:吊白块呈白色块状固体成结晶性粉状,易溶于水,微溶于乙醇,常温时较为稳定,高温下下具有强还原性:120℃以上会分解产生甲醛、二氧化硫和硫化氢等有毒气体。
回答下列问题:
(1)“反应Ⅰ”发生后溶液的pH=4.1,则反应I的产物是__。
(2)设计反应Ⅱ后向反应Ⅲ中继续通入SO2的目的是得到NaHSO3过饱和溶液,从而生成Na2S2O5,则反应Ⅲ中发生反应的化学方程式为__。
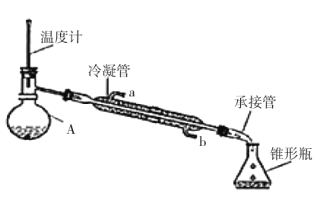
(3)“反应Ⅳ”加热的方式最好选用__(填“直接加热”或“水浴加热”);其反应的化学方程式为__。
(4)“过滤”得到的滤液蒸发浓缩时不能在敞口容器中进行,原因是__;洗涤时中的洗涤剂最好选择__(填字母序号)。
A.水 B.无水乙醇 C.稀氢氧化钠溶液
(5)由“滤渣”制备氧化锌的方法是__。
(6)一种测定吊白块中硫的质量分数的方法如下:称取ag产品溶于适量水中,加入稍过量的碘水(反应生成NaHSO4和HCOOH),充分反应后加入足量BaCl2溶液,过滤,滤渣经干燥后称得质量为bg。则产品中硫的质量分数为__(用含a、b的式子表示)。
【答案】NaHSO3、CO2 2NaHSO3= Na2S2O5+H2O 水浴加热 Na2S2O5+2Zn+2HCHO+3H2O![]() 2NaHSO2·HCHO+2Zn(OH)2↓ 吊白块具有强还原性,高温下易被空气中的氧气氧化 B 洗涤、(干燥)、煅烧(高温焙烧)
2NaHSO2·HCHO+2Zn(OH)2↓ 吊白块具有强还原性,高温下易被空气中的氧气氧化 B 洗涤、(干燥)、煅烧(高温焙烧) ![]()
【解析】
(1)Na2SO3溶液呈碱性, NaHSO3 溶液呈酸性;
(2)NaHSO3脱水生成Na2S2O5;
(3)“反应Ⅳ”反应温度为95℃;根据流程图可知Na2S2O5、Zn、HCHO反应生成NaHSO2·HCHO、Zn(OH)2;
(4)吊白块常温时较为稳定、高温下具有强还原性;吊白块微溶于乙醇;
(5)氢氧化锌加热分解为氧化锌;
(6)加入足量BaCl2溶液,过滤,bg滤渣为BaSO4,根据硫元素守恒计算。
(1)“反应I”发生后溶液的pH=4.1,溶液呈酸性,说明SO2和纯碱反应的产物是NaHSO3,则反应I的产物是NaHSO3、CO2;
(2)NaHSO3脱水生成Na2S2O5,反应的方程式是2NaHSO3=Na2S2O5+H2O;
(3)“反应IV”反应温度为95℃,加热的方式最好选用水浴加热;根据流程图可知Na2S2O5、Zn、HCHO反应生成NaHSO2·HCHO、Zn(OH)2反应方程式是Na2S2O5+2Zn+2HCHO+3H2O![]() 2NaHSO2·HCHO+2Zn(OH)2↓;
2NaHSO2·HCHO+2Zn(OH)2↓;
(4)吊白块常温时较为稳定、高温下具有强还原性,高温下易被空气中的氧气氧化,所以“过滤”得到的滤液蒸发浓缩时不能在敞口容器中进行;吊白块微溶于乙醇,洗涤时,洗涤剂最好用无水乙醇,选B;
(5)氢氧化锌加热分解为氧化锌,由“滤渣”制备氧化锌的方法是洗涤、(干燥)、煅烧(高温焙烧);
(6)加入足量BaCl2溶液,过滤,得到bgBaSO4,硫元素的质量为![]() ,根据硫元素守恒,ag产品中硫元素的质量为
,根据硫元素守恒,ag产品中硫元素的质量为![]() ,硫元素质量分数为
,硫元素质量分数为![]() ÷ag=
÷ag=![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】“一碳化学”是指以含一个碳原子的化合物(如CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)![]() NH2COONH4(s) H1
NH2COONH4(s) H1
反应II:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) H3=-86.98kJ/mol
CO(NH2)2(s)+H2O(g) H3=-86.98kJ/mol
请回答下列问题:
①反应I的H1=__kJ/mol。
②反应II一般在__(填“高温或“低温")条件下有利于该反应的进行。
③一定温度下,在体积固定的密闭容器中按计量比投料进行反应I,下列能说明反应达到了平衡状态的是__(填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(NH3)=v逆(CO2)
D.容器内混合气体的密度不再变化
(2)将CO2和H2按物质的量之比为1:3充入一定体积的密闭容器中,发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) H。测得CH3OH的物质的量在不同温度下随时间的变化关系如图所示。
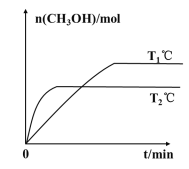
①根据图示判断H__0(填“>”或“<”)。
②一定温度下,在容积均为2L的两个密闭容器中,按如下方式加入反应物,10min后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2 cmolCH3OH(g)、cmolH2O(g)(a、b、c均不为零) |
若甲容器平衡后气体的压强为开始时的0.8倍,则反应10min内甲容器中以CH3OH(g)表示的化学反应速率为__,此温度下的化学平衡常数为__(保留两位小数);要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为__。
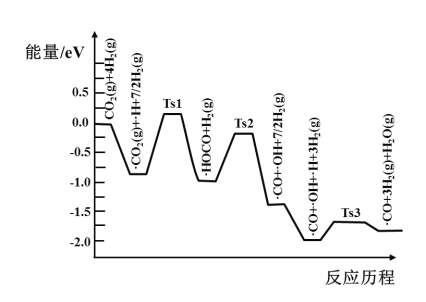
(3)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会__(填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为__。
CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会__(填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为__。