题目内容
【题目】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
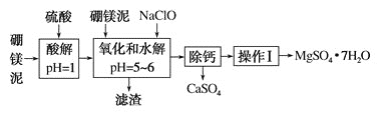
根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸900 mL,配制时所用的玻璃仪器除了烧杯、玻璃棒、量筒外,还需________________。
(2)加入的NaClO可将Mn2+氧化为MnO2 ,反应中无气体产生,反应的离子方程式为:________________。还有一种离子也会被NaClO氧化,反应的离子方程式为_______________________。
(3)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:___________________。
(4)已知MgSO4、CaSO4的溶解度如下表:
温度/℃ | 40 | 50 | 60 | 70 |
S(MgSO4)/g | 30.9 | 33.4 | 35.6 | 36.9 |
S(CaSO4)/g | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4的混合溶液中的CaSO4除去,根据上表数据,可确定操作步骤为蒸发结晶、_______________________(填操作名称)。
【答案】胶头滴管,100mL容量瓶 ![]()
![]() 取少量滤液于试管中,加入KSCN溶液,若不变红,则除尽 趁热过滤
取少量滤液于试管中,加入KSCN溶液,若不变红,则除尽 趁热过滤
【解析】
⑴实验中需用1 mol·L-1的硫酸900 mL,没有900mL的容量瓶,只能用1000mL容量瓶。
⑵加入的NaClO可将Mn2+氧化为MnO2 ,反应中无气体产生,说明生成了氯离子,反应的离子方程式为:ClO- + Mn2+ +H2O= MnO2 + Cl- +2H+,还有一种离子也会被NaClO氧化,亚铁离子也被次氯酸钠氧化生成铁离子和氯离子,其反应的离子方程式为2Fe2++ClO- + 2H+= 2Fe3+ + Cl-+H2O。
⑶在“除钙”前,需检验滤液中Fe3+是否被除尽,主要用KSCN溶液来检验铁离子。
⑷根据上表数据,硫酸钙温度越高溶解度越低,因此要趁热过滤。
⑴实验中需用1 mol·L-1的硫酸900 mL,没有900mL的容量瓶,只能用1000mL容量瓶,因此配制时所用的玻璃仪器除了烧杯、玻璃棒、量筒外,还需胶头滴管,100mL容量瓶。
⑵加入的NaClO可将Mn2+氧化为MnO2 ,反应中无气体产生,说明生成了氯离子,反应的离子方程式为:ClO- + Mn2+ +H2O= MnO2 + Cl- +2H+,还有一种离子也会被NaClO氧化,亚铁离子也被次氯酸钠氧化生成铁离子和氯离子,其反应的离子方程式为2Fe2++ClO- + 2H+= 2Fe3+ + Cl-+H2O,故答案为:ClO- + Mn2+ +H2O= MnO2 + Cl- +2H+;2Fe2++ClO-+ 2H+= 2Fe3+ + Cl-+H2O。
⑶在“除钙”前,需检验滤液中Fe3+是否被除尽,主要用KSCN溶液来检验铁离子,故答案为:取少量滤液于试管中,加入KSCN溶液,若不变红,则除尽。
⑷根据上表数据,硫酸钙温度越高溶解度越低,因此操作步骤为蒸发结晶、趁热过滤,故答案为:趁热过滤。