题目内容
下列离子方程式正确的是( )
| A、NaHS溶液中HS-水解:HS-+H2O?S2-+H3O+ |
| B、氯化铵水解:NH4++H2O?NH3?H2O+H+ |
| C、向NaHCO3 溶液中加入过量的Ca(OH)2溶液:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32- |
| D、碳酸钠溶液显碱性的原因:CO32-+2H2O?H2 CO3+2OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硫氢根离子水解生成硫化氢和氢氧根离子;
B.铵根离子水解生成一水合氨和氢离子;
C.二者反应生成碳酸钙、氢氧化钠和水;
D.碳酸根离子分步水解,第一步水解生成碳酸氢根离子和氢氧根离子.
B.铵根离子水解生成一水合氨和氢离子;
C.二者反应生成碳酸钙、氢氧化钠和水;
D.碳酸根离子分步水解,第一步水解生成碳酸氢根离子和氢氧根离子.
解答:
解:A.硫氢根离子水解生成硫化氢和氢氧根离子,离子方程式为HS-+H2O?H2S+HO-,故A错误;
B.铵根离子水解生成一水合氨和氢离子,离子方程式为NH4++H2O?NH3?H2O+H+,故B正确;
C.二者反应生成碳酸钙、氢氧化钠和水,离子方程式为HCO3-+OH-+Ca2+=CaCO3↓+H2O,故C错误;
D.碳酸根离子分步水解,第一步水解生成碳酸氢根离子和氢氧根离子,离子方程式为CO32-+H2O?HCO3-+OH-,故D错误;
故选B.
B.铵根离子水解生成一水合氨和氢离子,离子方程式为NH4++H2O?NH3?H2O+H+,故B正确;
C.二者反应生成碳酸钙、氢氧化钠和水,离子方程式为HCO3-+OH-+Ca2+=CaCO3↓+H2O,故C错误;
D.碳酸根离子分步水解,第一步水解生成碳酸氢根离子和氢氧根离子,离子方程式为CO32-+H2O?HCO3-+OH-,故D错误;
故选B.
点评:本题考查了离子方程式正误判断,明确物质的性质及离子之间的反应是解本题关键,注意多元弱酸根离子和多元弱碱阳离子水解方程式的区别,为易错点.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
将2mol SO2和1mol O2充入一容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g),下列哪些量不再变化时,并不能说明化学反应已达平衡状态( )
| A、混合气体的密度 |
| B、混合气体的压强 |
| C、混合气体的总物质的量 |
| D、混合气体的平均相对分子质量 |
根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A、金属性 Li<Na |
| B、非金属性 O>S |
| C、还原性 Mg<Al |
| D、得电子能力 Se>As |
下列离子方程式错误的是( )
| A、小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-=CO32-+H2O |
| B、澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
| C、Cl2与水反应生成盐酸和次氯酸Cl2+H2O=2H++Cl-+ClO- |
| D、硫酸与氢氧化钡溶液反应:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓ |
用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
A、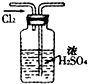 干燥氯气 |
B、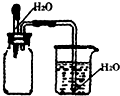 检验气体是否易溶于水 |
C、 制取并收集氨气 |
D、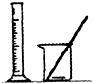 配制50mL 0.10mol?L-1 KI溶液 |
“保护环境,就是保护人类自己.”下列环境问题与产生的主要原因不相符的是( )
①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NO2等引起的
③“酸雨”主要是由空气中CO2浓度增大引起的
④“白色污染”主要是由聚苯乙烯塑料等引起的
⑤“温室效应”主要是由空气中CO2浓度增大引起的
⑥“赤潮”主要是由水体中P、N等元素过量引起的.
①“臭氧空洞”主要是大量使用氟氯代烃等引起的
②“光化学烟雾”主要是由NO2等引起的
③“酸雨”主要是由空气中CO2浓度增大引起的
④“白色污染”主要是由聚苯乙烯塑料等引起的
⑤“温室效应”主要是由空气中CO2浓度增大引起的
⑥“赤潮”主要是由水体中P、N等元素过量引起的.
| A、只有①② | B、只有②③⑤ |
| C、全部 | D、只有③ |
下列说法中正确的是( )
| A、HNO3的摩尔质量为63g |
| B、标况时22.4升氧气约为1mol |
| C、一个氮原子的实际质量约为1g |
| D、64g SO2中含有1mol O |
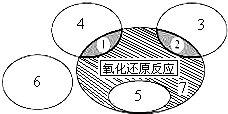 (1)如图是课本中“四种基本反应类型与氧化还原反应的关系”图,“H2+CuO
(1)如图是课本中“四种基本反应类型与氧化还原反应的关系”图,“H2+CuO