题目内容
下列离子方程式错误的是( )
| A、小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-=CO32-+H2O |
| B、澄清石灰水中通入过量的CO2:CO2+OH-=HCO3- |
| C、Cl2与水反应生成盐酸和次氯酸Cl2+H2O=2H++Cl-+ClO- |
| D、硫酸与氢氧化钡溶液反应:2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成碳酸钠和水;
B.反应生成碳酸氢钙;
C.反应生成盐酸和HClO,HClO在离子反应中保留化学式;
D.反应生成硫酸钡和水,符合离子的配比.
B.反应生成碳酸氢钙;
C.反应生成盐酸和HClO,HClO在离子反应中保留化学式;
D.反应生成硫酸钡和水,符合离子的配比.
解答:
解:A.小苏打溶液中加入过量的烧碱溶液的离子反应为HCO3-+OH-=CO32-+H2O,遵循电荷守恒和原子守恒,故A正确;
B.澄清石灰水中通入过量的CO2的离子反应为CO2+OH-=HCO3-,故B正确;
C.Cl2与水反应生成盐酸和次氯酸的离子反应为Cl2+H2O=H++Cl-+HClO,故C错误;
D.硫酸与氢氧化钡溶液反应的离子反应为2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓,故D正确;
故选C.
B.澄清石灰水中通入过量的CO2的离子反应为CO2+OH-=HCO3-,故B正确;
C.Cl2与水反应生成盐酸和次氯酸的离子反应为Cl2+H2O=H++Cl-+HClO,故C错误;
D.硫酸与氢氧化钡溶液反应的离子反应为2H++2OH-+Ba2++SO42-=2H2O+BaSO4↓,故D正确;
故选C.
点评:本题考查离子反应的书写,为高考常见题型,把握离子反应中保留化学式的物质即可解答,注意电荷守恒的应用,注重基础知识的考查,题目难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相等(不考虑水解),且SO42-的物质的量浓度为9mol/L,则此溶液最多溶解Mg的质量为( )
| A、24g | B、18g |
| C、21.6g | D、14.4g |
下列离子方程式正确的是( )
| A、NaHS溶液中HS-水解:HS-+H2O?S2-+H3O+ |
| B、氯化铵水解:NH4++H2O?NH3?H2O+H+ |
| C、向NaHCO3 溶液中加入过量的Ca(OH)2溶液:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32- |
| D、碳酸钠溶液显碱性的原因:CO32-+2H2O?H2 CO3+2OH- |
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、40g SO2气体所占的体积为11.2L |
| B、7.1g Cl2与水反应转移电子数为0.2NA |
| C、1mol?L-1的CH3COONa溶液中,CH3COO-离子数小于NA |
| D、常温常压下,32g O2和O3的混合气体含氧原子数为2NA |
下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同 |
| B、常温下1mol?L-1的CH3COOH溶液与1mol?L-1的NaOH溶液等体积混合,所得混合液中[Na+]>[CH3COO-]>[H+]>[OH-] |
| C、物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,[NH4+]前者小于后者 |
| D、常温下,某溶液中由水电离出的[H+]为1.0×10-5mol?L-1,则此溶液可能是盐酸,也可能是NH4Cl溶液 |
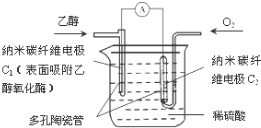 生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应方程式为:C2H5OH+3H2O-12e-=2CO2+12H+.下列说法不正确的是( )
生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应方程式为:C2H5OH+3H2O-12e-=2CO2+12H+.下列说法不正确的是( )| A、C1极为电池负极,C2极为电池正极 |
| B、C2极的电极反应式为O2+4H++4e-=2H2O |
| C、该生物燃料电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O |
| D、电池放电过程中电解质溶液的pH不变 |