题目内容
用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
A、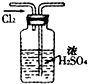 干燥氯气 |
B、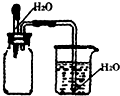 检验气体是否易溶于水 |
C、 制取并收集氨气 |
D、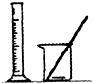 配制50mL 0.10mol?L-1 KI溶液 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.干燥装置中导气管应该遵循“长进短出”原则;
B.能产生压强差的装置能检验气体是否易溶于水;
C.氨气有刺激性气味,能污染大气;
D.量筒不能用于配置溶液.
B.能产生压强差的装置能检验气体是否易溶于水;
C.氨气有刺激性气味,能污染大气;
D.量筒不能用于配置溶液.
解答:
解:A.干燥装置中导气管应该遵循“长进短出”原则,否则易排出浓硫酸,故A错误;
B.如果气体极易溶于水,会导致集气瓶中压强急剧减小,外界大气压不变,则烧杯中的水会进入导管,如果该气体不易溶于水,则不会产生该现象,所以能检验该气体是否极易溶于水,故B正确;
C.氨气有刺激性气味,能污染大气,所以收集氨气时在试管底部放置棉花,故C错误;
D.量筒不能用于配置溶液,配制一定物质的量浓度溶液用容量瓶配制,故D错误;
故选B.
B.如果气体极易溶于水,会导致集气瓶中压强急剧减小,外界大气压不变,则烧杯中的水会进入导管,如果该气体不易溶于水,则不会产生该现象,所以能检验该气体是否极易溶于水,故B正确;
C.氨气有刺激性气味,能污染大气,所以收集氨气时在试管底部放置棉花,故C错误;
D.量筒不能用于配置溶液,配制一定物质的量浓度溶液用容量瓶配制,故D错误;
故选B.
点评:本题考查了实验方案评价,涉及气体的干燥、气体的收集、仪器的使用等知识点,根据气体的性质、气体的溶解性、仪器的使用方法即可解答,氨气的制取原理是高考热点,题目难度不大.

练习册系列答案
相关题目
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①澄清石灰水中通过量的CO2 ②向Fe(OH)3胶体中逐滴加入过量的稀硫酸
③向AgNO3溶液中逐滴加入过量氨水 ④向硅酸钠溶液中逐滴加入过量的盐酸.
①澄清石灰水中通过量的CO2 ②向Fe(OH)3胶体中逐滴加入过量的稀硫酸
③向AgNO3溶液中逐滴加入过量氨水 ④向硅酸钠溶液中逐滴加入过量的盐酸.
| A、②④ | B、③④ | C、④ | D、①③ |
下列离子方程式正确的是( )
| A、NaHS溶液中HS-水解:HS-+H2O?S2-+H3O+ |
| B、氯化铵水解:NH4++H2O?NH3?H2O+H+ |
| C、向NaHCO3 溶液中加入过量的Ca(OH)2溶液:2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32- |
| D、碳酸钠溶液显碱性的原因:CO32-+2H2O?H2 CO3+2OH- |
在一定温度下,一恒容容器中发生反应2A2(g)+B2(g)?2AB(g),该反应达到平衡状态的标志是( )
| A、单位时间生成n mol的A2同时生成n mol的AB |
| B、容器内的总压强不随时间变化 |
| C、容器内的气体密度不随时间变化 |
| D、单位时间内生成n mol的A2同时生成n mol的B2 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、62g Na2O溶于水后所得溶液中含有的O2-数为NA |
| B、标准状况下,NA个三氧化硫分子所占据的体积约是22.4L |
| C、常温常压下,16g甲基(-13CH3)所含的中子数为7NA |
| D、10L0.1mol?L-1的Na2CO3溶液中,Na+、CO32-总数为3NA |
表中物质的分类正确的一组是( )
| A | B | C | D | |
| 电解质 | NH3 | Na2CO3 | NH4NO3 | Fe(OH)3 |
| 混合物 | 漂白粉 | 明矾 | 铝热剂 | 冰水混合物 |
| 酸性氧化物 | CO2 | NO2 | SO3 | CO |
| 酸 | HClO | CH3COOH | H2SO4 | HNO3 |
| A、A | B、B | C、C | D、D |
金属铈(稀土元素)性质活泼.铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2.下列说法正确的是( )
| A、铈溶于氢碘酸的化学方程式可表示为:Ce+4HI═CeI4+2H2↑ |
| B、用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+ |
| C、在一定条件下,电解熔融状态的CeO2制Ce,在阳极获得铈 |
| D、四种铈的核素58136Ce、58138Ce、58140Ce、58142Ce,它们互称为同素异形体 |