题目内容
7.下列对应的表达方式错误的是( )| A. | Cl-的结构示意图: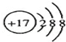 | B. | 氢氧根离子的电子式: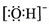 | ||
| C. | ${\;}_{6}^{12}$C的质量数为12 | D. | HClO的结构式:H-Cl-O |
分析 A.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构;
B.氢氧根离子为带有1个负电荷的阴离子,电子式中需要标出所带电荷及原子的最外层电子;
C.元素符号的左上角表示质量数、左下角表示质子数;
D.次氯酸的中心原子为O原子,分子中不存在氢氯键.
解答 解:A.氯离子的核电荷数为17,最外层为8个电子,Cl-的结构示意图为: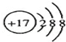 ,故A正确;
,故A正确;
B.氢氧根离子为阴离子,氢氧根离子的电子式为: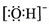 ,故B正确;
,故B正确;
C.该碳原子的质量数为12、质子数为6,故C正确;
D.次氯酸分子的中心原子为O,次氯酸正确的结构式为:H-O-Cl,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,注意掌握电子式、离子结构示意图、元素符号、结构式等化学用语的书写原则,试题培养了学生规范答题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 11.2L甲烷含有的氢原子数为2NA | |
| B. | 1mol氧气在化学反应中得到的电子数一定为4NA | |
| C. | 28g丙烯中含有的碳氢键的数目为4NA | |
| D. | 1mol/L的硝酸中含有的硝酸根离子的数目为4NA |
2.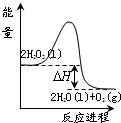 过氧化氢一定条件下可发生分解:2H2O2(l)═2H2O(l)+O2(g),其能量变化如图所示,下列说法正确的是( )
过氧化氢一定条件下可发生分解:2H2O2(l)═2H2O(l)+O2(g),其能量变化如图所示,下列说法正确的是( )
 过氧化氢一定条件下可发生分解:2H2O2(l)═2H2O(l)+O2(g),其能量变化如图所示,下列说法正确的是( )
过氧化氢一定条件下可发生分解:2H2O2(l)═2H2O(l)+O2(g),其能量变化如图所示,下列说法正确的是( )| A. | 该分解反应为吸热反应 | |
| B. | 2molH2O2具有的能量小于2molH2O和1molO2所具有的总能量 | |
| C. | 加入MnO2或FeCl3均可提高该分解反应的速率 | |
| D. | 其他条件相同时,H2O2溶液的浓度越大,其分解速率越慢 |
6.分子式为C5H10O2的羧酸共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 种 |
3.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A. | SO2和Si | B. | CO2和CH4 | C. | CsCl和H2SO4 | D. | CCl4和KCl |
4.下列有关实验说法错误的是( )
| A. | 在0.1mol/LK2Cr2O4溶液中,滴加3滴浓硫酸,K2Cr2O4溶液颜色会改变 | |
| B. | 在做温度对反应速率的影响实验时,应该将Na2S2O3和稀硫酸分别加热到设定温度再混合 | |
| C. | 恒温恒容已达H2(g)+I2(g)?2HI(g)平衡的容器中,充入少量HI(g),容器中气体颜色不变 | |
| D. | 不断读取数据,直到出现下降,取最大值,即为中和反应反应热的测定中混合溶液的最高温度 |
 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极、洗涤、干燥、称量,电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极、洗涤、干燥、称量,电极增重1.6g.请回答下列问题: