题目内容
3. 有机物A的分子式为C2H4,可能发生以下系列转化:
有机物A的分子式为C2H4,可能发生以下系列转化:己知B、D是生活中常见的两种有机物,请回答以下问:
(1)B分子中官能团的名称是羟基,D分子中官能团的符号是-COOH.
(2)A→B的化学方程式:CH2═CH2+H2O$→_{加热、加压}^{催化剂}$CH3CH2OH.
反应类型是加成反应..
(3)B→E的化学方程式:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
1molB与1mol D能否完全反应生成1mol不能(填“能”或“不能”),其理由是酯化反应可逆,反应物不能完全转化为乙酸乙酯.
分析 有机物A分子式为C2H4,则A为CH2═CH2,A与水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C进一步氧化生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3,据此解答.
解答 解:有机物A分子式为C2H4,则A为CH2═CH2,A与水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C进一步氧化生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3,
(1)B为CH3CH2OH,含有的官能团为羟基,D为CH3COOH,含官能团为-COOH,故答案为:羟基;-COOH;
(2)A为CH2═CH2,A与水发生加成反应生成B为CH3CH2OH,化学方程式为CH2═CH2+H2O$→_{加热、加压}^{催化剂}$CH3CH2OH,
故答案为:CH2═CH2+H2O$→_{加热、加压}^{催化剂}$CH3CH2OH;加成反应;
(3)乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3,化学方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,酯化反应可逆,反应物不能完全转化为乙酸乙酯,故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;不能;酯化反应可逆,反应物不能完全转化为乙酸乙酯.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸、酯的性质等,比较基础,有利于基础知识的巩固,注意酯化反应是可逆反应.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
14.乙酸橙花酯的结构简式如图所示,下列叙述中正确的是( )
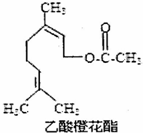

| A. | 该有机物分子式为C12H20O2 | |
| B. | 能发生加成反应和取代反应 | |
| C. | 不能使酸性KMnO4溶液褪色 | |
| D. | 1mol该有机物最多能与2mol NaOH反应 |
18.硼元素在自然界主要以硼酸.硼酸盐和硼硅酸盐存在.请回答下列问题:
(1)硼元素是ⅢA族的第一个元素,原子结构示意图为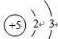 ,天然硼元素有两种稳定同位素10B、11B,其相对原子质量分别为10和11,它们的相对丰度分别为20%和80%,硼元素的平均相对质量为10.8.
,天然硼元素有两种稳定同位素10B、11B,其相对原子质量分别为10和11,它们的相对丰度分别为20%和80%,硼元素的平均相对质量为10.8.
(2)硼酸(H3BO3)是一元弱酸,工业上用硼砂(Na2B4O7•10H2O)制备硼酸晶体的流程如图甲:
不同温度下硼酸的溶解度见下表:
①写出硼砂溶液和稀硫酸反应的离子方程式5H2O+B4O72-+2H+=4H3BO3.
②上述流程中获得粗硼酸晶体的操作Ⅰ为降温结晶(冷却热饱和溶液)、过滤,进一步将粗硼酸晶体提纯的方法是重结晶.
③25℃时0.1mol/L硼酸溶液的PH约为5.1,则其电离常数K约为10-9.2.
(3)硼酸在加热过程中发生分解的失重曲线如图乙所示.
①硼酸从开始加热到107℃时,发生反应的化学方程式为H3BO3═HBO2+H2O.
②硼酸加热到160℃得到的固体的化学式为H2B4O7.(B元素的相对原子质量按11计算)
(4)NaBH4由于H元素显-1价,具有强还原性,是有机化学上的万能还原剂.在碱性条件下电解NaBO2溶液可以制得NaBH4,其反应方程式为NaBO2+2H2O=2O2↑+NaBH4,则阴极反应式为BO2-+6H2O+8e-=BH4-+8OH-.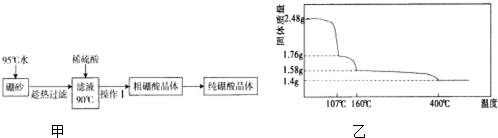
(1)硼元素是ⅢA族的第一个元素,原子结构示意图为
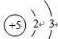 ,天然硼元素有两种稳定同位素10B、11B,其相对原子质量分别为10和11,它们的相对丰度分别为20%和80%,硼元素的平均相对质量为10.8.
,天然硼元素有两种稳定同位素10B、11B,其相对原子质量分别为10和11,它们的相对丰度分别为20%和80%,硼元素的平均相对质量为10.8.(2)硼酸(H3BO3)是一元弱酸,工业上用硼砂(Na2B4O7•10H2O)制备硼酸晶体的流程如图甲:
不同温度下硼酸的溶解度见下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 2.7 | 5.0 | 8.7 | 14.8 | 23.8 |
②上述流程中获得粗硼酸晶体的操作Ⅰ为降温结晶(冷却热饱和溶液)、过滤,进一步将粗硼酸晶体提纯的方法是重结晶.
③25℃时0.1mol/L硼酸溶液的PH约为5.1,则其电离常数K约为10-9.2.
(3)硼酸在加热过程中发生分解的失重曲线如图乙所示.
①硼酸从开始加热到107℃时,发生反应的化学方程式为H3BO3═HBO2+H2O.
②硼酸加热到160℃得到的固体的化学式为H2B4O7.(B元素的相对原子质量按11计算)
(4)NaBH4由于H元素显-1价,具有强还原性,是有机化学上的万能还原剂.在碱性条件下电解NaBO2溶液可以制得NaBH4,其反应方程式为NaBO2+2H2O=2O2↑+NaBH4,则阴极反应式为BO2-+6H2O+8e-=BH4-+8OH-.

7.以下离子:①H+ ②Cl- ③Al3+ ④K+ ⑤SO42- ⑥OH- ⑦NO3-⑧NH4+中,不影响水的电离平衡的是( )
| A. | ②④⑤⑦ | B. | ②④⑥⑦ | C. | ①⑤⑥⑦ | D. | ②④⑥⑧ |
8.化学与生活密切相关.下列说法中不正确的是( )
| A. | “雨后彩虹”是一种与光学和胶体性质相关的自然现象 | |
| B. | 纯银器表面在空气渐渐变暗,是电化学腐蚀所致 | |
| C. | 右图电流表指针偏转,有电流通过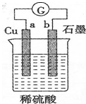 | |
| D. | 在食品中科学使用食品添加剂对人体无害 |
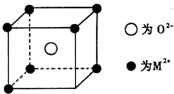 已知MO与CsCl的结构相似(如图2所示),MO晶体的密度为p g•cm-3,NA为阿伏加德罗常数,相邻的两个M2+的核间距为acm.写出Cs基态原子的价电子排布式6s1,MO的相对分子质量可以表示为ρa3 NA.
已知MO与CsCl的结构相似(如图2所示),MO晶体的密度为p g•cm-3,NA为阿伏加德罗常数,相邻的两个M2+的核间距为acm.写出Cs基态原子的价电子排布式6s1,MO的相对分子质量可以表示为ρa3 NA.