题目内容
钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,该反应的反应物与生成物有CO、Pd、H2O、HCl、PdCl2和一种未知物质X。下列说法错误的是
| A.未知物质X为CO2,属于氧化产物 |
| B.每转移1mol e-时,生成2mol X |
| C.反应中PdCl2作氧化剂,被还原 |
| D.还原性:CO>Pd |
B
解析试题分析:CO为常见的还原剂,则钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,因此该反应中碳元素的化合价升高,Pd元素的化合价降低,结合质量守恒定律可知,发生反应的化学方程式为CO+PdCl2+H2O=CO2+Pd↓+2HC1。则A、由反应可知,X物质为CO2,属于氧化产物,故A正确;B、X物质为CO2,因此碳元素的化合价从+2价升高到+4价,失去2个电子,所以反应中转移的电子为1 mo1时,生成0.5molCO2,故B错误;C、反应中PdCl2作氧化剂,得电子而被还原,故C正确;D.氧化还原反应中还原剂的还原性强于还原产物的。反应中CO作还原剂,Pd为还原产物,因此还原性为:CO>Pd,故D正确,答案选B。
考点:考查氧化还原反应的有关判断和计算

 计算高手系列答案
计算高手系列答案实验室可以用高锰酸钾与浓盐酸反应制取氯气,反应的化学方程式如下:
2KMn04+16HCl(浓) = 2KCl+5Cl2↑+2MnCl2+8H20
对于该反应,下列说法正确的是
| A.HCl是氧化剂 | B.是非氧化还原反应 |
| C.反应中锰元素被还原 | D.反应中氢元素的化合价升高 |
下列物质性质的比较,正确的是
| A.热稳定性:Na2CO3>NaHCO3>H2CO3 |
| B.熔点:K>Na>Li |
| C.同条件下,同浓度溶液的pH值:NaHCO3>Na2CO3 |
| D.还原性:S2->Br->I- |
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4==2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3==2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中均为硫元素被氧化 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
| C.氧化性:MnO2>SO42->IO3->I2 |
| D.反应①、②中生成等量的I2时转移电子数比为1∶5 |
下列陈述I、II正确并且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | H2O2、SO2都能使酸性高锰酸钾褪色 | 前者表现出还原性后者表现出漂白性 |
| B | 纯银器表面在空气中渐渐变暗 | 发生了化学腐蚀 |
| C | SiO2能与氢氟酸及碱反应 | SiO2是两性氧化物 |
| D | BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 | 说明Ksp(BaSO4)大于Ksp(BaCO3) |
已知:还原性HSO—3>I—,氧化性IO—3>I2。在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法不正确的是
| A.0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ |
| B.a点时消耗NaHSO3的物质的量为0.12mol |
| C.当溶液中I—与I2的物质的量之比为5:2时,加入的KIO3为0.18mol |
| D.b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2 |
除废气NO的反应原理为:2CO+2NO=N2+2CO2有关该反应的说法不正确的是 ( )
| A.反应中CO为氧化剂 |
| B.反应中NO被还原 |
| C.在反应生成1 mol N2时,转移的电子为4 mol |
| D.CO和NO都是无色有毒气体 |
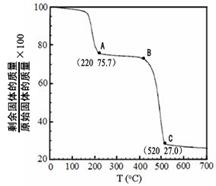
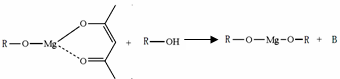
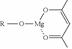 ,它可发生如下反应:
,它可发生如下反应: