题目内容
10.下列有关硬水及其软化的说法中错误的是( )| A. | 离子交换法可以软化硬水 | |
| B. | 生产、生活使用的天然水必须经软化 | |
| C. | 硬水中含有较多Ca2+、Mg2+ | |
| D. | 加热可使暂时硬水中的Ca2+生成CaCO3沉淀 |
分析 硬水中含有较多量的Ca2+、Mg2+等离子,人长期饮用危害健康.硬水加热会有较多的水垢,可用离子交换法软化硬水.
解答 解:A.离子交换法可以减小水中Ca2+、Mg2+等离子的含量,降低硬水的硬度,软化硬水,故A正确;
B.如生活、生产使用的天然水硬度较小,可不用软化,故B错误;
C.硬水是指硬度高于8度的水为硬水,含较多的钙镁化合物,故C正确;
D.硬水经过煮沸或蒸馏以后,水里所含的碳酸氢钙或碳酸氢镁就会分解成不溶于水的碳酸钙和难溶于水的氢氧化镁沉淀.这些沉淀物析出,水的硬度就可以降低,从而使硬度较高的水得到软化,故D正确.
故选B.
点评 本题考查硬水与软化,侧重考查学生运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀,该有机样品可能是( )
| A. | 乙酸 | B. | 乙醇 | ||
| C. | 乙醛 | D. | 甲醇和丙三醇的混合物 |
1.下列实验中操作、现象、结论对应关系正确的一组是( )
| 选 项 | 操作 | 现象 | 结论 |
| A | 向稀的苯酚水溶液中滴加浓溴水 | 生成白色沉淀 | 产物三溴苯酚不溶于水 |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸酸化,再加入硝酸银溶液 | 生成淡黄色沉淀 | 溴乙烷中含有溴元素 |
| D | 将溴水加入苯中并充分振荡 | 溴水褪色 | 苯与溴发生了取代反应 |
| A. | A | B. | B | C. | C | D. | D |
18.将一定量的A、B物质充入一密闭容器中,发生如下反应A(g)+3B(g)?2C(g),3min后测得C浓度为0.6mol•L-1,则此时间内用C表示的反应速率正确的是( )
| A. | 0.2mol•(L•s)-1 | B. | 0.2mol•(L•min)-1 | C. | 0.6mol•(L•min)-1 | D. | 0.3mol•(L•min)-1 |
5.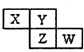 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | Z的离子半径小于Y的离子半径 | |
| B. | W的最高价氧化物对应水化物的酸性比Z的强 | |
| C. | Z的非金属性比Y的强 | |
| D. | X与Y形成的化合物都易溶于水 |
15.以海水为原料制取下列物质时,不需要经过氧化还原反应的是( )
| A. | 溴 | B. | 铀 | C. | 氯化镁 | D. | 氢氧化钠 |
2.实验室用Fe2+的废酸液(pH为1.7)制取氧化铁晶体的流程如图所示.下列说法错误的是( )
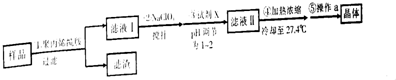

| A. | 步骤①中过滤操作需用到的玻璃仪器为玻璃棒、分液漏斗、烧杯 | |
| B. | 步骤②中搅拌操作可加快散热,减少FeCl3水解 | |
| C. | 步骤③中加入的试剂X为浓盐酸 | |
| D. | 步骤⑤中操作a为过滤、洗涤、干燥 |
19.能证明丙烯分子里含有一个碳碳双键的事实是( )
| A. | 丙烯分子里碳氢原子的个数比为1:2 | |
| B. | 丙烯完全燃烧生成的CO2和H2O的物质的量相等 | |
| C. | 丙烯能使酸性KMnO4溶液褪色 | |
| D. | 丙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质 |
20.NaH与水反应的化学方程式为NaH+H2O═NaOH+H2↑,在该反应中NaH( )
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |