题目内容
20.NaH与水反应的化学方程式为NaH+H2O═NaOH+H2↑,在该反应中NaH( )| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
分析 在反应NaH+H2O═NaOH+H2↑中,NaH中H的化合价为-1价,H2O中H的化合价为+1价,只有H元素的化合价发生变化.
解答 解:在反应NaH+H2O═NaOH+H2↑中,NaH中H的化合价为-1价,在反应中升高为0价,所以NaH为还原剂,故B正确.
故选:B.
点评 本题考查氧化还原反应,为高考常见题型,侧重于学生的分析能力和基础知识的考查,注意从化合价的角度解答该题,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列有关硬水及其软化的说法中错误的是( )
| A. | 离子交换法可以软化硬水 | |
| B. | 生产、生活使用的天然水必须经软化 | |
| C. | 硬水中含有较多Ca2+、Mg2+ | |
| D. | 加热可使暂时硬水中的Ca2+生成CaCO3沉淀 |
11.下列有关原子结构的说法中,正确的是( )
| A. | 决定元素种类的是--电子数 | |
| B. | 决定元素化学性质的是--原子的核外电子数 | |
| C. | 决定元素相对原子质量的是--中子数 | |
| D. | 决定元素周期表中原子序数的是--核电荷数 |
15.已知外电路中,电子由铜流向a极.有关图所示的装置分析合理一项是( )
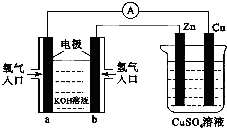

| A. | 该装置中Cu极为正极 | |
| B. | 当铜极的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L | |
| C. | b极反应的电极反应式为:H2-2e-═2H+ | |
| D. | 一段时间后锌片质量减少 |
5.某有机物能使溴水褪色,也能在一定条件下发生水解生成两种有机物,还能发生加聚反应生成高分子化合物,则此有机物中一定含有下列基团的组合是( )
①-CH3;②-OH;③-Cl;④-CHO;⑤-C2H3;⑥-COOH;⑦-COOCH3.
①-CH3;②-OH;③-Cl;④-CHO;⑤-C2H3;⑥-COOH;⑦-COOCH3.
| A. | ①③ | B. | ②⑥ | C. | ⑤⑦ | D. | ④⑤ |
9.下列表示式正确的是( )
| A. | 氨分子的电子式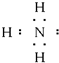 | B. | 氢氧根离子的电子式 | ||
| C. | 乙酸的结构简式 C2H4O2 | D. | 苯的实验式 C6H6 |
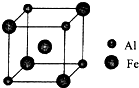 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.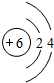 ,B与C形成的化合物的电子式为
,B与C形成的化合物的电子式为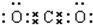 .
.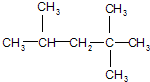 它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简
它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简 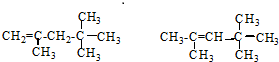 .
.