题目内容
15.以海水为原料制取下列物质时,不需要经过氧化还原反应的是( )| A. | 溴 | B. | 铀 | C. | 氯化镁 | D. | 氢氧化钠 |
分析 发生的反应中,存在元素的化合价变化,则为氧化还原反应;反之,不存在元素的化合价变化,则不是氧化还原反应,以此来解答.
解答 解:A.海水含有溴离子,用氯气氧化成溴单质,为氧化还原反应,故A不选;
B.海水中主要含铀离子,转化为铀,元素的化合价变化,是氧化还原反应,故B不选;
C.海水中存在镁离子,转化为沉淀后生成氯化镁,没有元素的化合价变化,不是氧化还原反应,故C选;
D.海水中主要含NaCl,电解法制备氢氧化钠,元素的化合价变化,是氧化还原反应,故D不选;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
6.下列方法中,不能用于实验室里制取氨气的是( )
| A. | 在烧瓶中将熟石灰和氯化铵混合,加水调成泥糊状后加热 | |
| B. | 将烧瓶中的浓氨水加热 | |
| C. | 加热试管中的氯化铵固体 | |
| D. | 将分液漏斗中的浓氨水滴入装有浓硫酸的烧瓶中 |
3.下列实验方法能达到实验目的是( )
| A. | 乙烯中含有S02杂质,可将混合气体通入酸性KMn04溶液以提纯 | |
| B. | 向淀粉溶液中加入少盘稀硫酸,加热4〜5min,待溶液冷却后加入含氢氧化钠的氢氧化铜悬浊液,加热至沸腾,若未见砖红色沉淀生成,说明淀粉未水解 | |
| C. | 通过钠、镁分别与冷水反应的剧烈程度,可以比较钠、镁的金属性强弱 | |
| D. | 向溴水中加入乙醇,充分振荡,可以将溴水中的Br2萃取出来 |
10.下列有关硬水及其软化的说法中错误的是( )
| A. | 离子交换法可以软化硬水 | |
| B. | 生产、生活使用的天然水必须经软化 | |
| C. | 硬水中含有较多Ca2+、Mg2+ | |
| D. | 加热可使暂时硬水中的Ca2+生成CaCO3沉淀 |
20.下列说法正确的是(NA为阿伏伽德罗常数的值)( )
| A. | 取1.06gNa2CO3溶于水,滴入2滴酚酞试液,用盐酸滴定至终点,所得溶液的Cl-数目约为0.01NA | |
| B. | 25℃时,将pH=2的醋酸溶液加水稀释100倍,所得溶液的H+数目约为10-4NA | |
| C. | 25℃时,向100mL1mol•L-1盐酸中通入0.1molNH3,所得溶液的H+数目为10-8NA | |
| D. | 0.1molAgCl和0.1molAgI混合后加入0.1L水中,所得溶液的c(Cl-)=c(I-) |
7.生活中的某些问题常常涉及化学知识.下列叙述错误的是( )
| A. | 用聚乳酸塑料代替聚乙烯塑料可减少白色污染 | |
| B. | 煤油、“乙醇汽油”、“生物柴油”都是碳氢化合物 | |
| C. | 为防治碘缺乏病,在食用盐中添加适量的碘酸钾 | |
| D. | 甘油可用作护肤保湿剂 |
4.关于氮的变化关系示意图如图:则下列说法不正确的是( )
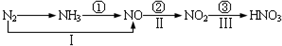

| A. | 路线①②③是工业生产硝酸的主要途径 | |
| B. | 路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 | |
| C. | 上述所有反应都是氧化还原反应 | |
| D. | 上述反应中①②③均属于氮的固定 |

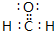 ,推测该分子的空间构型为平面三角形.
,推测该分子的空间构型为平面三角形.