题目内容
【题目】25℃时,在20mL0.1molL﹣1NaOH溶液中逐滴加入0.2molL﹣1的某一元弱酸HX溶液,曲线如图所示,有关粒子浓度关系的比较中,错误的是( )
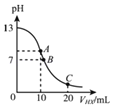
A.在A点:c(Na+)>c(OH﹣)>c(X﹣)>c(H+)
B.在B点:c(OH﹣)=c(H+)=c(Na+)=c(X﹣)
C.在C点:c(X﹣)>c(Na+)>c(H+)>c(OH﹣)
D.在C点:c(X﹣)+c(HX)=2c(Na+)
【答案】AB
【解析】
A.A点酸碱的物质的量相等,二者恰好完全反应生成NaX,X﹣水解导致溶液呈碱性,存在c(Na+)>c(X﹣),但是其水解程度较小,所以c(X﹣)>c(OH﹣),结合电荷守恒得, c(Na+)>c(X﹣)>c(OH﹣)>c(H+),故A错误;
B.溶液pH=7,溶液呈中性,则c(OH﹣)=c(H+),根据电荷守恒得c(Na+)=c(X﹣),水的电离程度很小,所以存在c(OH﹣)=c(H+)<c(Na+)=c(X﹣),故B错误;
C.C点溶液中溶质为等物质的量浓度的NaX、HX,溶液呈酸性,c(H+)>c(OH﹣),说明HX电离程度大于NaX水解程度,根据电荷守恒判断c(X﹣)>c(Na+),但是HX电离程度较小,所以存在c(X﹣)>c(Na+)>c(H+)>c(OH﹣),故C正确;
D.任何电解质溶液中都存在物料守恒,根据物料守恒得c(X﹣)+c(HX)=2c(Na+),故D正确;
故选:AB。

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案【题目】某研究小组将纯净的SO2气体缓缓的通入到盛有25mL0.1mol· L-1的Ba(NO3)2溶液中,得到BaSO4沉淀。为探究该反应中的氧化剂,该小组提出了如下假设:
假设Ⅰ:溶液中的NO3-;
假设Ⅱ:________________。
(1)该小组设计了以下实验验证了假设Ⅰ成立(为排除假设Ⅱ对假设Ⅰ的干扰,在配制下列实验所用溶液时,应___________________),请填写下表。
实验步骤 | 实验现象 | 结论 | |
实验① | 向盛有25mL0.1mol·L-1BaCl2溶液的烧杯中缓慢通入纯净的SO2气体 | ______ | 假设Ⅰ成立 |
实验② | 向盛有25mL0.1mol· L-1Ba(NO3)2溶液的烧杯中缓慢通入纯净的SO2气体 | ______ | |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图。V1时,实验②中溶液pH小于实验①的原因是(用离子方程式表示):________。

(3)验证假设Ⅱ。某同学设计了以下方案,请完成下列表格(可以不填满)。
实验步骤 | 实验现象 | 实验目的 | ||
实验③ | 同实验①步骤 | 同实验①的相关现象 | ______ | |
实验④ | ______ | ______ | ______ | |
(4)查资料知:H2SO3是二元酸(Kl=1.54×10-2,K2=1.02×10-7),请设计实验方案验证H2SO3是二元酸______(试剂及仪器自选)。
【题目】I。草酸(H2C2O4)与高锰酸钾在酸性条件下能够发生反应:
(实验1)甲同学用8.00 mL 0.001 mol/L KMnO4溶液与5.00 mL 0.01 mol/L H2C2O4溶液反应,研究不同条件对化学反应速率的影响。改变的条件如下:
组别 | KMnO4溶液 /mL | H2C2O4溶液 /mL | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 8.00 | 5.00 | 3.00 | 20 | |
Ⅱ | 8.00 | 5.00 | 3.00 | 30 | |
Ⅲ | 8.00 | 5.00 | 1.00 | 20 | 2.00 mL蒸馏水 |
(1)写出草酸(H2C2O4)与高锰酸钾溶液在酸性条件下反应的离子方程式________。
(2)上述进行实验Ⅰ、Ⅲ的目的是探究__________对化学反应速率的影响。
(实验2)乙同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
(3)针对上述现象,乙同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是_______的影响。
(4)若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是____(填字母)。
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
Ⅱ.用如图所示的装置进行中和热的测定实验,分别取![]() 的
的![]() 溶液、
溶液、![]() 的硫酸进行实验,回答下列问题:
的硫酸进行实验,回答下列问题:
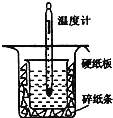
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是__________,除此之外,装置中的一个明显错误是__________。
(2)近似认为![]() 的NaOH溶液和
的NaOH溶液和![]() 的硫酸溶液的密度都是
的硫酸溶液的密度都是![]() ,中和后生成溶液的比热容
,中和后生成溶液的比热容![]() ,通过以下数据计算中和热△H=__________(结果保留小数点后一位)。
,通过以下数据计算中和热△H=__________(结果保留小数点后一位)。
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(3)上述实验数值结果与![]() 有偏差,产生偏差的原因可能是(填字母)_____。
有偏差,产生偏差的原因可能是(填字母)_____。
a.实验装置保温、隔热效果差
b.用温度计测定![]() 溶液起始温度后直接测定H2SO4溶液的温度
溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把![]() 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中
d.将以上四实验测量温度均纳入计算平均值