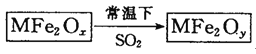题目内容
【题目】前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。回答下列问题:
(1)D2+的价层电子排布图为_____。
(2)四种元素中第一电离最小的是____,电负性最大的是____。(填元素符号)
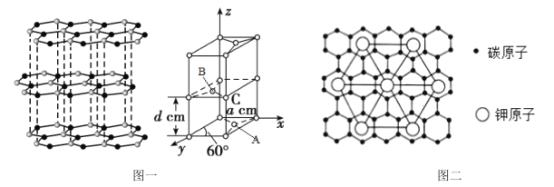
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
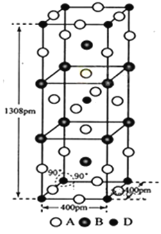
①该化合物的化学式为_____________;D的配位数为_______;
②列式计算该晶体的密度为___________g·cm-3。(列式并计算)
【答案】![]() K F K2NiF4 6
K F K2NiF4 6 ![]() =3.4
=3.4
【解析】
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,说明B、C、D为第四周期,则B为K,再根据前面信息得出A为F,C和D原子序数相差为2,则C为Fe,D为Ni。
(1)D为Ni,Ni为28号元素,价电子排布式为3d84s2,因此D2+的价层电子排布图为![]() ;故答案为:
;故答案为:![]() 。
。
(2)根据电离能同周期从左到右增大趋势,同主族从上到下逐渐减小,因此四种元素中第一电离最小的是K,电负性同周期从左到右逐渐增大,同主族从上到下逐渐减小,因此电负性最大的是F;故答案为:K;F。
(3)①根据晶胞计算A(F-)的个数![]() ,B(K+)的个数
,B(K+)的个数![]() ,D(Ni2+)的个数
,D(Ni2+)的个数![]() ,因此该化合物的化学式为K2NiF4;以顶点的D分析,其配位数是上下左右前后,共6;故答案为:K2NiF4;6。
,因此该化合物的化学式为K2NiF4;以顶点的D分析,其配位数是上下左右前后,共6;故答案为:K2NiF4;6。
②列式计算该晶体的密度为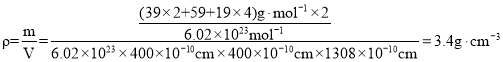 ;故答案为:
;故答案为: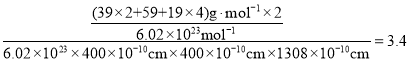 。
。

 名校课堂系列答案
名校课堂系列答案【题目】某铁的氧化物粉末可能含有FeO、Fe2O3中的一种或两种。某化学兴趣小组为验证该氧化物粉末的组成,做了如下实验:
(1)甲同学利用1mol/L的硫酸、KSCN溶液、酸性高锰酸钾溶液来确定其组成
编号 | 实验操作 | 实验现象与结论 |
① | 取少量粉末放入试管中,注入1mol/L的硫酸 | 粉末逐渐溶解,溶液呈黄绿色 |
② | 将①中所得溶液分成两份,向其中一份滴加几滴__________,振荡 | 若溶液________ ,说明有Fe2O3存在 |
③ | 向另一份溶液中加入少量__________,振荡 | 若溶液________ ,说明有FeO存在 |
(2)乙同学称取30.4g固体,按以下步骤进行实验:
步骤一 将固体置于烧杯中,加入1mol/L的硫酸将固体完全溶解
步骤二 往烧杯中先加入足量的氯水,充分反应后再加入足量的氢氧化钠溶液
步骤三 将步骤二所得的物质过滤洗涤后,灼烧至固体质量不再变化,得到32g红棕色固体
①步骤二中加入氯水的目的是__________________________________________;
②步骤三中沉淀洗涤的操作为__________________________________________;
③原固体中FeO和Fe2O3的物质的量之比为___________________。