题目内容
将纯锌片和纯铜片按如图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )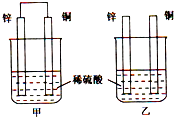

| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中正极的电极反应式为Zn-2e-=Zn2+ |
| C、两烧杯中氢离子浓度均减少 |
| D、产生气泡的速度甲比乙慢 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,总反应式为:Zn+H2SO4=ZnSO4+H2↑;乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑,以此进行分析.
解答:
解:A、甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,所以甲中铜片表面有气泡产生,故A错误;
B、甲中铜为正极,铜片上氢离子得电子生成氢气,正极的反应为:2H++2e-=H2↑,故B错误;
C、甲中铜片上氢离子得电子生成氢气,乙中锌和稀硫酸发生置换反应生成氢气,所以两烧杯的溶液中氢离子浓度均减小,故C正确;
D、甲中形成铜锌原电池加快了反应速率,所以产生气泡的速度甲比乙快,故D错误;
故选C.
B、甲中铜为正极,铜片上氢离子得电子生成氢气,正极的反应为:2H++2e-=H2↑,故B错误;
C、甲中铜片上氢离子得电子生成氢气,乙中锌和稀硫酸发生置换反应生成氢气,所以两烧杯的溶液中氢离子浓度均减小,故C正确;
D、甲中形成铜锌原电池加快了反应速率,所以产生气泡的速度甲比乙快,故D错误;
故选C.
点评:本题考查了置换反应和原电池的有关知识,题目难度不大,注意把握原电池的组成条件的工作原理.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列表示对应反应的离子方程式正确的是( )
| A、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | ||||
| B、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ | ||||
| C、碳酸氢钠的水解:HCO3-+H2O?CO32-+H3O+ | ||||
D、用惰性电极电解氯化镁溶液:2Cl-+2H2O
|
下列说法正确的是( )
| A、强电解质溶液的导电能力比弱电解质强 |
| B、难溶盐如:BaSO4、CaCO3、AgCl等是弱电解质,易溶性盐如:醋酸铵是强电解质 |
| C、在水溶液中是否完全电离是判断强弱电解质的依据 |
| D、二氧化硫溶于水可以导电,所以二氧化硫是电解质 |
复合物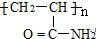 的单体是( )
的单体是( )
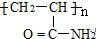 的单体是( )
的单体是( )A、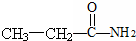 |
B、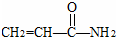 |
| C、CH2=CH2 |
D、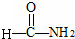 |
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A、该电池工作时电能转化为化学能 |
| B、该电池中电极a是正极 |
| C、该电池的总反应:2H2+O2═2H2O |
| D、外电路中电子由电极b通过导线流向电极a |
已知25℃时,Ksp(AgI)=8.5×10-17,Ksp(AgCl)=1.8×10-10,若在5mL含有KCl和KI均为0.01mol?L-1的溶液中,缓慢滴加8mL 0.01moL-1 AgNO3溶液,下列叙述正确的是( )
| A、混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | ||
| B、混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) | ||
| C、加入AgNO3溶液时首先生成AgCl沉淀 | ||
D、混合溶液中
|
关于苯的下列说法正确的是( )
| A、苯的分子是环状结构,其性质跟环烷烃相似 |
B、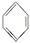 表示苯的分子结构,其中含有碳碳双键,因此苯的性质跟烯烃相同 表示苯的分子结构,其中含有碳碳双键,因此苯的性质跟烯烃相同 |
| C、苯的分子式是C6H6,分子中的C原子远没有饱和,因此能使溴水褪色 |
| D、苯环上的碳碳键的键能、键长介于单双键之间 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA |
| B、常温下,pH=1的H2SO4溶液中含有的H+的数目为0.1NA |
| C、标准状况下,2.24L SO3中含有硫原子的数目为NA |
| D、常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
某同学用一小块铝片和盐酸反应制取H2,实验现象如下表:
反应1~15min内,铝与盐酸的反应速率变化的可能原因是( )
| 时间 | 1min | 2min | 5min | 15min | 20min |
| 现象 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| A、该反应是放热反应,温度升高 |
| B、反应过程中盐酸的浓度增大 |
| C、随着反应的进行,铝片表面积变小 |
| D、Cl-离子是该反应的催化剂 |