��Ŀ����
��Na2SO3����������ҵSO2β����Ⱦ������һ������SO2β����Ⱦ�Ƚ���ӱ�ķ�������������ǣ��ٽ�����SO2����Ĺ���β��ͨ�뵽Na2SO3��Һ�У�ʹ�����պ���β���е�SO2���壻�ڽ�������SO2�������Һ���ȣ�����ʹ���е�SO2�����ݳ�����ЩSO2�������Ӧ������ȡH2SO4���÷�����Na2SO3����ѭ��ʹ�ã�������ɫ��ѧ�Ļ���ԭ�������������Ϣ����������⣺
��1��д���١��������Ļ�ѧ����ʽ
�� ��
�� ��
��2������10m3��0.1mol/L��Na2SO3��Һ��ÿ�����ձ�״���µĺ���SO2�����β��89.6m3���ﵽ�˱���״̬������ù���������β����SO2�������������Ƕ��٣�
��1��д���١��������Ļ�ѧ����ʽ
��
��
��2������10m3��0.1mol/L��Na2SO3��Һ��ÿ�����ձ�״���µĺ���SO2�����β��89.6m3���ﵽ�˱���״̬������ù���������β����SO2�������������Ƕ��٣�
���㣺�����������Ⱦ������
ר�⣺����Ԫ��
��������1��Na2SO3����SO2��Ӧ������ʽ��NaHSO3��NaHSO3���ȶ����ڼ����������ֽ⣬�ֱ�д����Ӧ�Ļ�ѧ����ʽ��
��2�����ݷ�Ӧ�Ļ�ѧ����ʽNa2SO3+SO2+H2O=2NaHSO3��������Ķ�����������ʵ�����Ȼ����������¶�����̼����������������ù���������β����SO2��������������
��2�����ݷ�Ӧ�Ļ�ѧ����ʽNa2SO3+SO2+H2O=2NaHSO3��������Ķ�����������ʵ�����Ȼ����������¶�����̼����������������ù���������β����SO2��������������
���
�⣺��1����Na2SO3����SO2��Ӧ������ʽ��NaHSO3����Ӧ�ķ���ʽΪNa2SO3+SO2+H2O=2NaHSO3��
�ʴ�Ϊ��Na2SO3+SO2+H2O=2NaHSO3��
��NaHSO3���ȶ����ڼ����������ֽ⣬��Ӧ�Ļ�ѧ����ʽΪ2NaHSO3
Na2SO3+SO2��+H2O��
�ʴ�Ϊ��2NaHSO3
Na2SO3+SO2��+H2O��
��2����μӷ�Ӧ��SO2�����ʵ���Ϊx
Na2SO3 +SO2+H2O=2NaHSO3
1 1mol
0.1mol/L��10��103L x
��ã�x=0.1mol/L��10��103L=1000mol��
�ù���������β����SO2������������Ϊ��
��100%=25%��
�𣺸ù���������β����SO2��������������25%��
�ʴ�Ϊ��Na2SO3+SO2+H2O=2NaHSO3��
��NaHSO3���ȶ����ڼ����������ֽ⣬��Ӧ�Ļ�ѧ����ʽΪ2NaHSO3
| ||
�ʴ�Ϊ��2NaHSO3
| ||
��2����μӷ�Ӧ��SO2�����ʵ���Ϊx
Na2SO3 +SO2+H2O=2NaHSO3
1 1mol
0.1mol/L��10��103L x
��ã�x=0.1mol/L��10��103L=1000mol��
�ù���������β����SO2������������Ϊ��
| 1000mol��22.4L/mol |
| 89.6��103L |
�𣺸ù���������β����SO2��������������25%��
���������⿼�����ʵ����ʼ���ѧ����ʽ�ļ��㣬��Ŀ�Ѷ��еȣ�ע�����ճ������ʵ����ʼ���Ӧԭ�����ܹ����ݷ�Ӧ����ʽ���мĻ�ѧ���㣮

��ϰ��ϵ�д�
�����Ŀ
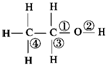 �Ҵ���һ�������£�������������Ӧʱ����ѧ������λ����ͼ�еģ�������
�Ҵ���һ�������£�������������Ӧʱ����ѧ������λ����ͼ�еģ�������| A���ڢ� | B���ڢ� | C���٢� | D���ۢ� |
���з�Ӧ�������ȷ�Ӧ���ǣ�������
| A������������������������ |
| B��������������ȼ�� |
| C�����������������Ȼ�茶��巴Ӧ |
| D������������Һ�������к� |
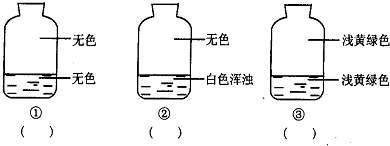
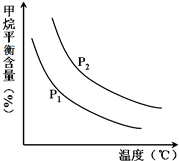
�����Լ��У����������ڲ���ƿ�е��ǣ�������
| A��Ũ���� | B������� |
| C��Ũ����������Һ | D����������Һ |
 ���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol��
���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol��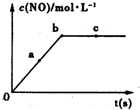 ��Ԫ�صĵ��ʼ��仯������о���Ӧ���ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ����ҵ���������Ҫ��Ӧ֮һ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-akJ?mol-1��a��0��
��Ԫ�صĵ��ʼ��仯������о���Ӧ���ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ����ҵ���������Ҫ��Ӧ֮һ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-akJ?mol-1��a��0��