��Ŀ����
����������ɶ�����Ԫ����ɵ��մɲ��ϣ���һ���Թ��ۼ����������ʣ��������¡�������������Ժõ��������ʣ������Ʊ����ֲ��ϵ���ʼԭ�ϣ�Ҳ�����������Ҫ�ɷ֣��Ʊ�ʱ��ȡ̼�Ȼ�ԭ����������������̿�۰�һ��������ϣ�������N2�����м��ȵ�һ���¶ȼ��ɵõ��Ϳ�ȼ�������������ԭ�Ӹ���֮�Ⱦ�Ϊ1��1.8.2g��������������������Һ��Ͽ��Եõ���ɫ��Һ������������״����4.48L�����죮
��1���ҵĻ�ѧʽΪ ��д������һ����; ��
��2���ľ�������Ϊ ��д��̼�Ȼ�ԭ�������ƼĻ�ѧ����ʽ ��
��3����ҵ�Ʊ��Ĺ����п��ܺ��е������� ��
��4��������ĽṹʽΪ ��д����������������������Һ��Ӧ�Ļ�ѧ����ʽΪ ����֤��Һ�������ʵ�ʵ�鷽��Ϊ ��
��1���ҵĻ�ѧʽΪ
��2���ľ�������Ϊ
��3����ҵ�Ʊ��Ĺ����п��ܺ��е�������
��4��������ĽṹʽΪ
���㣺������ƶ�
ר�⣺�ƶ���
�����������Ʊ����ֲ��ϵ���ʼԭ�ϣ�Ҳ�����������Ҫ�ɷ֣�����ΪAl2O3���Ʊ�ʱ��ȡ̼�Ȼ�ԭ����������������̿�۰�һ��������ϣ�������N2�����м��ȵ�һ���¶ȼ��ɵõ��Ϳ�ȼ�������������ԭ�Ӹ���֮�Ⱦ�Ϊ1��1������Al2O3+N2+3C
2AlN+3CO�����ΪAlN����ΪCO��8.2g�ף�AlN��������������������Һ��Ͽ��Եõ���ɫ��Һ������������״����4.48L�����죬��Ϊ������n���ף�=n���죩=0.2mol���Դ������
| ||
���
�⣺�����Ʊ����ֲ��ϵ���ʼԭ�ϣ�Ҳ�����������Ҫ�ɷ֣�����ΪAl2O3���Ʊ�ʱ��ȡ̼�Ȼ�ԭ����������������̿�۰�һ��������ϣ�������N2�����м��ȵ�һ���¶ȼ��ɵõ��Ϳ�ȼ�������������ԭ�Ӹ���֮�Ⱦ�Ϊ1��1������Al2O3+N2+3C
2AlN+3CO�����ΪAlN����ΪCO��8.2g�ף�AlN��������������������Һ��Ͽ��Եõ���ɫ��Һ������������״����4.48L�����죬��Ϊ����
��1��������������֪����ΪAl2O3���۵�ߣ����������²��ϣ��ʴ�Ϊ��Al2O3�����²��ϣ�
��2����ΪAlN���Թ��ۼ����������ʣ��������¡�������������Ժõ��������ʣ���Ϊԭ�Ӿ��壬̼�Ȼ�ԭ�������ƼĻ�ѧ����ʽΪAl2O3+3C+N2
2AlN+3CO��
�ʴ�Ϊ����Al2O3+3C+N2
2AlN+3CO��
��3����Al2O3+3C+N2
2AlN+3CO��֪����Ӧ���й������ʣ�࣬��������Al4C3���Ʊ��Ĺ����п��ܺ��е�������Al2O3��C��Al4C3�ȣ�
�ʴ�Ϊ��Al2O3��C��Al4C3�ȣ�
��4����ĽṹʽΪ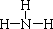 ����������������������Һ��Ӧ�Ļ�ѧ����ʽΪAlN+NaOH+H2O=NaAlO2+NH3������֤��Һ�������ʵ�ʵ�鷽��Ϊȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
����������������������Һ��Ӧ�Ļ�ѧ����ʽΪAlN+NaOH+H2O=NaAlO2+NH3������֤��Һ�������ʵ�ʵ�鷽��Ϊȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
�ʴ�Ϊ��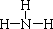 ��AlN+NaOH+H2O=NaAlO2+NH3����ȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
��AlN+NaOH+H2O=NaAlO2+NH3����ȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
| ||
��1��������������֪����ΪAl2O3���۵�ߣ����������²��ϣ��ʴ�Ϊ��Al2O3�����²��ϣ�
��2����ΪAlN���Թ��ۼ����������ʣ��������¡�������������Ժõ��������ʣ���Ϊԭ�Ӿ��壬̼�Ȼ�ԭ�������ƼĻ�ѧ����ʽΪAl2O3+3C+N2
| ||
�ʴ�Ϊ����Al2O3+3C+N2
| ||
��3����Al2O3+3C+N2
| ||
�ʴ�Ϊ��Al2O3��C��Al4C3�ȣ�
��4����ĽṹʽΪ
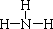 ����������������������Һ��Ӧ�Ļ�ѧ����ʽΪAlN+NaOH+H2O=NaAlO2+NH3������֤��Һ�������ʵ�ʵ�鷽��Ϊȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
����������������������Һ��Ӧ�Ļ�ѧ����ʽΪAlN+NaOH+H2O=NaAlO2+NH3������֤��Һ�������ʵ�ʵ�鷽��Ϊȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2���ʴ�Ϊ��
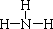 ��AlN+NaOH+H2O=NaAlO2+NH3����ȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
��AlN+NaOH+H2O=NaAlO2+NH3����ȡ������Һ�����Թ��У���μ���ϡ���ᣬ���Ȳ�����ɫ��������ʧ��˵��ΪNaAlO2��
���������⿼��������ƶϣ�Ϊ��Ƶ���㣬���������Ʊ����ֲ��ϵ���ʼԭ�ϣ�Ҳ�����������Ҫ�ɷ����ƶ���Ϊ����ͻ�ƿڣ���ȷ�����ķ�Ӧ�����ʵ������ƶϼ��ɣ����ط������ƶ������Ŀ��飬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
�����Ŀ
���й��ڰ�����˵����ȷ���ǣ�������
| A����������Ũ�������Ҳ������ˮCaCl2���� |
| B��NH3�ǵ���ʣ�����ˮ�ܵ��� |
| C��NH3����ʹ����ĺ�ɫʯ����ֽ���� |
D��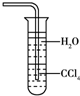 ��ˮ����NH3����ͼװ�ÿɷ�ֹ���� |
������Һ�У���ʯ��ˮ ��Na2S��Һ ��KMnO4��Һ ����ˮ ���ữ��Ba��NO3��2��Һ ��Ʒ����Һ����������SO2��CO2������ǣ�������
| A���� | B���٢� | C���٢ڢ� | D���ڢܢ� |
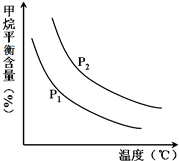 ���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol��
���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol��