题目内容
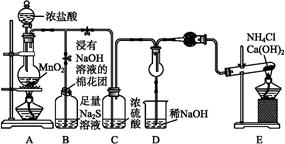
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、炭粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,并设计出相关实验流程图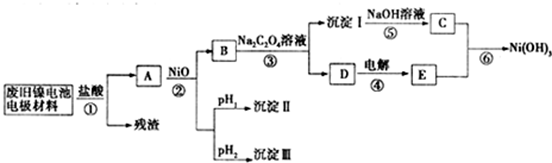
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-33 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
回答下列问题:
(1)根据表数据判断步骤②依次析出沉淀Ⅱ 和沉淀Ⅲ (填化学式),则pH1 pH2(填填“>”、“=”或“<”),控制两种沉淀析出可利用 。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则反应③的化学方程式是 .第③步反应后,过滤沉淀时需要的玻璃仪器有 .若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因 、 。
(3)④中阳极反应产生的气体E为 ,验证该气体的试剂为 。
(4)试写出反应⑥的离子方程式_____________________________________________
(1)Fe(OH)3 Al(OH)3 < C (4分)
(2)NiCl2+Na2C2O4+2H2O=NiC2O4·2H2O+2NaCl (2分)
烧杯、漏斗、玻璃棒;(3分) 滤纸破损、过滤液的液面高于滤纸的边缘(2分)
(3)Cl2 湿润的淀粉碘化钾试纸(2分)
(4)2Ni(OH)2+Cl2+2OH—=2Nii(OH)3+2Cl—(2分)
解析试题分析:(1)根据金属氢氧化物的Kap及沉淀析出的理论pH,结合流程图可知,先沉淀的是三价铁离子,随后沉淀的是三价铝离子,控制两种沉淀析出必须准确测定溶液PH,所以用PH计测定,故答案为:沉淀Ⅱ是Fe(OH)3,沉淀Ⅲ是Al(OH)3 ,PH1<PH2,C;
(2)由溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O和流程中的变化可知沉淀为溶解度小的NiC2O4·2H2O,所以根据转化关系写出化学方程式;在过滤装置中用到的玻璃仪器和注意问题,根据装置和操作步骤写出NiCl2+Na2C2O4+2H2O=NiC2O4.2H2O↓+2NaCl,故答案为:NiCl2+Na2C2O4+2H2O=NiC2O4.2H2O↓+2NaCl; 漏斗、玻璃棒、烧杯;玻璃棒划破滤纸、滤液超过滤纸边缘;
(3)D溶液时氯化钠溶液,电解反应方程式2NaCI+2H2O 2NaOH+Cl2↑+H2↑,E气体为Cl2,故答案:Cl2,淀粉碘化钾溶液;
2NaOH+Cl2↑+H2↑,E气体为Cl2,故答案:Cl2,淀粉碘化钾溶液;
(4)根据转化关系和Ni2+沉淀的PH推知,加入氢氧化钠的主要目的是把NiC2O4·2H2O沉淀转化为Ni(OH)2沉淀,为了使沉淀完全转化,加入的氢氧化钠溶液应过量,根据镍元素化合价变化,结合氧化还原反应的规律写出离子方程2Ni(OH)2+2OH-+Cl2=2Ni(OH)3 +2Cl-;
考点:考查金属回收的基本方法、难溶电解质的溶解与沉淀应用、沉淀转化的条件,铝、铁、镍元素化合物的化学性质,离子的沉淀PH范围,物质的分离、提纯的方法,实验基本操作等。

Ⅰ.铜铁及其化合物在日常生活中应用广泛,某研究性学习小组用粗铜(含杂质Fe)与过量氯气反应得固体A,用稀盐酸溶解A,然后加试剂调节溶液的pH后得溶液B,溶液B经系列操作可得氯化铜晶体,请回答:
(1)固体A用稀盐酸溶解的原因是 __。
(2)检验溶液B中是否存在Fe3+的方法是 __。
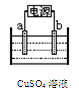
(3)已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是 。
Ⅱ.常温下,某同学将稀盐酸和氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | 氨水物质的量浓度/(mol·L-1) | 盐酸物质的量浓度/(mol·L-1) | 混合溶液pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>7 |
请回答:
(4)从第①组情况分析,该组所得混合溶液中由水电离出的c(H+)= __mol·L-1;从第②组情况表明,c __(填“>”“<”或“=”)0.2 mol·L-1;从第③组情况分析可知,混合溶液中c(NH4+) __(填“>”“<”或“=”)c(NH3·H2O)。
(5)写出以下四组溶液NH4+浓度由大到小的顺序 __> __> __> __(填选项编号)。
A.0.1 mol·L-1 NH4Cl
B.0.1 mol·L-1 NH4Cl和0.1 mol·L-1 NH3·H2O
C.0.1 mol·L-1 NH3·H2O
D.0.1 mol·L-1 NH4Cl和0.1 mol·L-1 HCl
1 L某混合溶液,可能含有的离子如下表。
| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32—、AlO2— |
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。则该溶液中一定不含有的离子是_________________________。
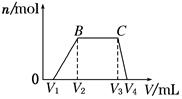
(2)BC段离子方程式为_______________________________________________。
(3)V1、V2、V3、V4之间的关系为__________________________________________。
(4)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题。
| Cl2的体积(标准状况) | 2.8 L | 5.6 L | 11.2 L |
| n(Cl-) | 1.25 mol | 1.5 mol | 2 mol |
| n(Br-) | 1.5 mol | 1.4 mol | 0.9 mol |
| n(I-) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为_________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为_____________________________。
(1)某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 | CO32—、SiO32—、AlO2—、Cl- |
| 阳离子 | Al3+、Cu2+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y的体积(V)的关系如图所示。
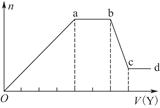
①若Y是盐酸,则溶液中含有的金属阳离子是_________________________________,
ab段发生反应的总离子方程式为___________________________________
表中Oa段与Y溶液反应的离子的物质的量之比为__________[要标明离子符号,如n(Na+)]。
②若Y是NaOH溶液,则bc段反应的离子方程式为______________________________
若不考虑离子的水解因素,忽略H+和OH-的影响,且溶液中只存在4种离子,则它们的离子个数比为___________________________________[按阳离子在前,阴离子在后,高价在前,低价在后的顺序排列]。
(2)锡为第ⅣA族元素,锡的单质和化合物与某些物质的化学性质上有许多相似之处。已知锡元素具有如下性质:
Sn4++Sn=2Sn2+;
2Sn2++O2+4H+=2Sn4++2H2O;
2H++SnO22—
 Sn(OH)2
Sn(OH)2 Sn2++2OH-。
Sn2++2OH-。试回答:
①锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应变化,试写出有关反应的离子方程式:______________________________________,
②将①中溶液蒸干后继续加热所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是(分子式)__________。
③若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2, 该碱是__________。
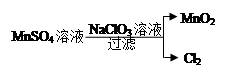
 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。