题目内容
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2 mol/L醋酸,曲线如右图所示,有关叙述错误的是

A.在A、B间任一点,溶液中都有c(Na+)>c(CH3COO-) > c(OH-)>c(H+)
B.在B点,a >12.5,且c(Na+)=c(CH3COO-)
C.在C点,c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
D.在D点,c(CH3COO-)+c(CH3COOH)=0.2mol/L

A.在A、B间任一点,溶液中都有c(Na+)>c(CH3COO-) > c(OH-)>c(H+)
B.在B点,a >12.5,且c(Na+)=c(CH3COO-)
C.在C点,c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
D.在D点,c(CH3COO-)+c(CH3COOH)=0.2mol/L
AD
试题分析:若加入醋酸溶液很少,则可能出现c(Na+)> c(OH-)>c(CH3COO-) > c(H+),A错误;当加入12.5mL醋酸时,醋酸与氢氧化钠溶液恰好中和生成醋酸钠溶液,溶液呈碱性,而B点pH=7,说明醋酸过量,a>12.5,溶液中电荷守恒式为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),由pH=7得c(Na+)=c(CH3COO-),B正确;C点为醋酸和醋酸钠混合溶液,电荷守恒式为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),C正确;D点为等物质的量CH3COOH与CH3COONa的混合溶液,由物料守恒得c(CH3COO-)+c(CH3COOH)=0.1mol/L,D错误。
点评:向氢氧化钠溶液中滴加醋酸,一般情况下,pH>7时,c(Na+)>c(CH3COO-) > c(OH-)>c(H+),但要注意特殊情况,即醋酸加入量很少时,c(Na+)> c(OH-)>c(CH3COO-) > c(H+)。

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
 之比为2:1
之比为2:1 ;b.
;b. ;c.
;c. ;d.
;d. 。其溶液物质的量浓度由小到大顺序为d、b、c、a
。其溶液物质的量浓度由小到大顺序为d、b、c、a 溶液中滴加NaOH溶液至溶液pH=7,则
溶液中滴加NaOH溶液至溶液pH=7,则

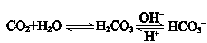 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表: