题目内容
人体血液里存在重要的酸碱平衡: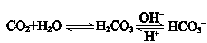 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
下列说法不正确的是
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
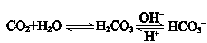 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:| c(HCO3-) ∶c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
D
试题分析:人体血液pH保持在7.35~7.45,人体的酸碱平衡:
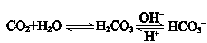
从该平衡可以看到人体的酸碱对是碳酸和碳酸氢根,人体血液pH小于7.35时碳酸会转化成碳酸氢根,使酸性降低,当人体血液pH大于7.45,碳酸氢根会转化成碳酸增大酸度。
所以正常人体血液中,HCO3-的水解程度大于电离程度;人体血液酸中毒时,只要增加碳酸氢根即可缓解,所以可注射NaHCO3溶液当然可以缓解酸中毒;从pH随c(HCO3-)∶c(H2CO3)变化关系表:
| c(HCO3-) ∶c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
可以看到PH=6.10时c(H2CO3)=c(HCO3-) ,此后随着PH值的增大,碳酸氢根迅速增大,所以pH=7.00的血液中,c(H2CO3)<c(HCO3-) ;pH=7.40的血液中,c(HCO3-)∶c(H2CO3)=20.0
只能说明血液中的HCO3-远大于H2CO3但并不能说明HCO3-的水解程度一定大于H2CO3的电离程度,所以D错。故选D。
点评:抓住人体的酸碱平衡:
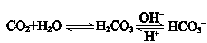 和pH随c(HCO3-)∶c(H2CO3)变化关系表的数据信息,考查了学生对给定条件平衡的分析,数据信息的分析能力。
和pH随c(HCO3-)∶c(H2CO3)变化关系表的数据信息,考查了学生对给定条件平衡的分析,数据信息的分析能力。
练习册系列答案
相关题目

 )与c(SO
)与c(SO )之比是 ( )
)之比是 ( )