题目内容
【题目】机动车排放的污染物主要有碳氢化合物、一氧化碳和氮氧化物等。
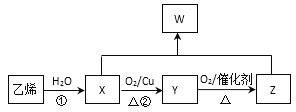
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知: C(s)+O2(g) = CO2(g) △H1 = 393.5kJ·mol1
2C(s)+O2(g) = 2CO(g) △H2 = 221.0 kJ·mol1
N2(g)+O2(g) = 2NO(g) △H 3 =+180.5 kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_________________________。
(2)研究CO和NO的催化反应,用气体传感器测得在某温度下、一定体积的密闭容器中,不同时间NO和CO浓度如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(______)4mol·L1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(______)3mol·L1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
① 前4 s内的平均反应速率υ(CO) =______mol·L1·s1。
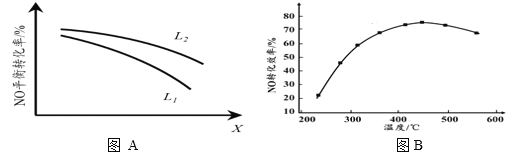
② L、X可分别代表压强或温度。下图A表示L一定时,NO(g)的平衡转化率随X的变化关系。X代表的物理量是______。判断L1、L2的大小关系,并简述理由:______________________________。
(3)实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2) ·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数______(填“>”、“
②若在2 L的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆 =___________。(保留一位小数)
II. 有人利用反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率是不是对应温度下的平衡转化率及判断理由是________________________;
N2(g)+CO2(g) ΔH = 34.0 kJ·mol1,用活性炭对NO进行吸附。现在密闭容器中加入足量的C和一定量的NO气体并在催化剂作用下发生反应,经相同时间测得NO的转化率随温度的变化如图B所示。由图可知最高转化率对应温度为450℃。低于450℃时,NO的转化率是不是对应温度下的平衡转化率及判断理由是________________________;
【答案】2NO(g)+2CO(g) =N2(g)+2CO2(g) ![]() H =746.5 kJ·mol1 2.25 ×104 温度 L2>L1 该反应为气体体积减小的反应,相同温度下压强增大,NO转化率增大 < 0.5 不是,该反应是放热反应 平衡转化率随温度升高而降低
H =746.5 kJ·mol1 2.25 ×104 温度 L2>L1 该反应为气体体积减小的反应,相同温度下压强增大,NO转化率增大 < 0.5 不是,该反应是放热反应 平衡转化率随温度升高而降低
【解析】
I.应用盖斯定律,第1个方程式减去第2个方程式,再减第3个方程式得到CO和NO在催化剂作用下生成N2的热化学方程式。
(2)①前4 s内的平均反应速率υ(CO) =![]() 。
。
②NO(g)的平衡转化率随X的变化关系,转化率在减小,说明是升高温度,平衡向吸热反应移动即逆向移动,因此X代表的物理量是温度,L代表的物理量是压强,从L1到L2,转化率增大,说明是正向移动,即加压,因此L2>L1,原因是该反应为气体体积减小的反应,相同温度下压强增大,NO转化率增大。
(3)①达到平衡后,仅升高温度,平衡逆向移动,逆反应速率增加的程度大于正反应速率增加的程度,因此k正增大的倍数 < k逆增大的倍数。
②根据方程式建立 “三步走”
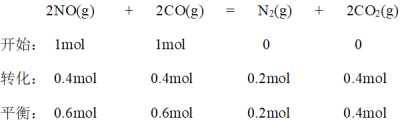
达到平衡时:v正= v逆,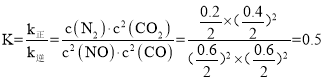 。
。
II.低于450℃时,是正在建立平衡的阶段,高于450℃时,是NO的转化率随温度升高而降低,因此该反应为放热反应。
I.第1个方程式减去第2个方程式,再减第3个方程式得到CO和NO在催化剂作用下生成N2的热化学方程式是2NO(g)+2CO(g) =N2(g)+2CO2(g) ![]() H =746.5 kJ·mol1,故答案为:2NO(g)+2CO(g) =N2(g)+2CO2(g)
H =746.5 kJ·mol1,故答案为:2NO(g)+2CO(g) =N2(g)+2CO2(g) ![]() H =746.5 kJ·mol1。
H =746.5 kJ·mol1。
(2)①前4 s内的平均反应速率υ(CO) =![]() ,故答案为:2.25×104。
,故答案为:2.25×104。
②NO(g)的平衡转化率随X的变化关系,转化率在减小,说明是升高温度,平衡向吸热反应移动即逆向移动,因此X代表的物理量是温度,L代表的物理量是压强,从L1到L2,转化率增大,说明是正向移动,即加压,因此L2>L1,原因是该反应为气体体积减小的反应,相同温度下压强增大,NO转化率增大,故答案为:L2>L1;该反应为气体体积减小的反应,相同温度下压强增大,NO转化率增大。
(3)①达到平衡后,仅升高温度,平衡逆向移动,逆反应速率增加的程度大于正反应速率增加的程度,因此k正增大的倍数 < k逆增大的倍数,故答案为:< 。
②
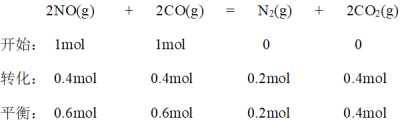
达到平衡时:v正= v逆,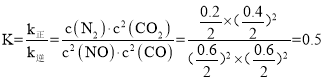 ,故答案为 0.5。
,故答案为 0.5。
II.低于450℃时,是正在建立平衡的阶段,高于450℃时,是NO的转化率随温度升高而降低,因此该反应为放热反应,故答案为:不是,该反应是放热反应;平衡转化率随温度升高而降低。

【题目】欲配制250mL0.1molL-1的稀盐酸,实验室的浓盐酸密度为1.25gcm-3,质量分数为36.5%。
请回答下列问题:
(1)配制稀盐酸时下表中不需要使用的仪器有___(填序号),还缺少的仪器为___、___(写仪器名称)。
序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
仪器 |
|
|
|
|
|
|
(2)需要量取浓盐酸的体积为___mL。
(3)配制该溶液的操作顺序是:D→___→___→___→___→B(用字母符号表示,每个字母符号只用一次)。
A.用30mL蒸馏水洗涤烧杯和玻璃棒各2~3次,将洗涤液全部注入容量瓶中并轻轻摇动
B.将容量瓶盖紧,振满,摇匀
C.将已恢复至室温的盐酸沿玻璃棒注入所选用的容量瓶中
D.用量筒准确量取所需体积的浓盐酸,将其沿玻璃棒注入烧杯中,再向烧杯中加入少量蒸馏水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
E.改用胶头滴管滴加蒸馏水,使溶液的凹液面恰好与容量瓶的刻度线相切
F.继续往容量瓶中小心地滴加蒸馏水,直到液面接近刻度线1~2cm处
(4)在定容时,液面高于刻度线,则所配溶液的浓度将___(选填“偏高”或“偏低”),该如何处理?___。