题目内容
【题目】23℃时,有体积相同的四种溶液:①pH=3的 CH3COOH溶液②pH=3的盐酸③pH=11的氨水④pH=11的NaOH溶液。下列说法不正确的是
A.用蒸馏水将①稀释则 ![]() 增大
增大
B.等体积②和③的溶液混合后,溶液呈酸性
C.将③逐渐滴入②中,水的电离程度先增大后减小
D.③和④分别用②中和,消耗②的体积:③>④
【答案】B
【解析】
醋酸和一水合氨都是弱电解质,溶液中存在电离平衡,氯化氢和氢氧化钠是强电解质,完全电离。
A、用蒸馏水将CH3COOH溶液稀释, c(CH3COO-)、c(CH3COOH) 均减小,但是醋酸的电离平衡向右移动,c(CH3COOH)减小的程度更大,故![]() 增大,故A正确;
增大,故A正确;
B、pH=11的氨水与pH=3的盐酸溶液等体积混合,氨水平衡状态下的氢氧根离子浓度和盐酸溶液中的氢离子浓度相同恰好反应,氨水又电离出铵根离子和氢氧根离子,所以氨水有剩余,所以溶液pH大于7,故B错误;
C、将氨水逐渐滴入盐酸中,先反应生成氯化铵,铵根水解促进水的电离,而到后面氨水过量,又会抑制水的电离,所以水的电离程度先增大后减小,故C正确。
D、pH相等的氨水和氢氧化钠,氨水浓度大于氢氧化钠,且二者都是一元碱,中和酸的能力与碱的物质的量成正比,等体积等pH的氨水和氢氧化钠,氨水的物质的量大于氢氧化钠,所以③和④分别用等浓度的盐酸溶液中和,消耗盐酸溶液的体积:③>④,故D正确。
答案选B。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题
(1)煤的气化的主要化学反应方程式为________________
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为____________
(3)利用水煤气合成二甲醚的三步反应如下
①2H2(g)+CO(g)=CH3OH(g) △H=-90.8kJ.mo-1
②2CH3OH(g)= CH3OCH3(g)+ H2O(g) △H=-235kJ.mo-1
③CO(g)+H2O(g)=O2(g)+H2(g) △H=-413kJ.mo-1
总反应:3H2(g)+3CO(g)= CH3OCH3(g)+CO2(g)的△H=___________
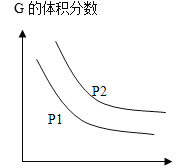
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是____(填字母代号)![]()
a. 高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加Co的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)= CH3OCH3(g)+ H2O(g)某温度下的平衡常数为400.此温度下,在2L密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
物质的量(mol) | 0.88 | 1.2 | 1.2 |
①加入的CH3OH的起始浓度为_________
②比较此时正、逆反应速率的大小:v正________v逆(填少”、“<”或“=”)
③若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率a(CH3OH)=_________c(CH3OCH3)=____________