题目内容
【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图所示。
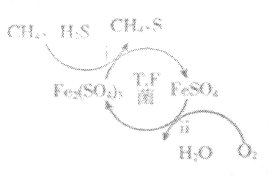
(1)过程i中H2S发生了___(填“氧化”或“还原”)反应。
(2)过程ii的离子方程式是___。
(3)已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
Fe2+氧化速率/(g·L-1·h-1) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
请结合以上信息,判断工业脱硫应选择的最佳pH范围,并说明原因:___。
II.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(4)①该过程的热化学方程式是___。
②比较压强p1和p2的大小关系:p1___p2(选填“>”“<”或“=”)。
III.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
IV.H2提纯:将CO2和H2分离得到H2的过程示意图如图。

(5)①吸收池中发生反应的离子方程式是___。
②结合电极反应式,简述K2CO3溶液的再生原理:___。
【答案】氧化 4Fe2++O2+4H+![]() 4Fe3++2H2O 1.5≤pH<1.9,当pH大于1.9时,Fe3+开始沉淀,导致Fe2+和Fe3+浓度均下降,会降低反应速率。pH小于1.5时,T.F菌活性较低,反应速率减慢 CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+204kJmol-1 > CO2+H2O+CO32-=2HCO3- 阴极反应:2H2O+2e=H2↑+2OH-,OH-+HCO3-=CO32-+H2O;阳极反应:4H2O-4e=O2↑+4H+,H++HCO3-=CO2+H2O,阳极区多余的K+经阳离子交换膜进入阴极区,使K2CO3溶液得以再生
4Fe3++2H2O 1.5≤pH<1.9,当pH大于1.9时,Fe3+开始沉淀,导致Fe2+和Fe3+浓度均下降,会降低反应速率。pH小于1.5时,T.F菌活性较低,反应速率减慢 CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+204kJmol-1 > CO2+H2O+CO32-=2HCO3- 阴极反应:2H2O+2e=H2↑+2OH-,OH-+HCO3-=CO32-+H2O;阳极反应:4H2O-4e=O2↑+4H+,H++HCO3-=CO2+H2O,阳极区多余的K+经阳离子交换膜进入阴极区,使K2CO3溶液得以再生
【解析】
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图2;
(1)硫化氢被硫酸铁氧化生成单质硫;
(2)过程Ⅱ是亚铁离子酸性条件下被氧气氧化生成铁离子;
(3)1.5≤PH<1.9,当PH大于1.9时,Fe3+开始沉淀,导致Fe3+、Fe2+离子浓度均下降,降低反应速率,PH<1.5时,TF菌活性较低;
Ⅱ.(4)①在催化剂的作用下,水蒸气将CH4氧化生成一氧化碳和水蒸气,图中反应的焓变△H=2582kJ/mol-2378kJ/mol=204kJ/mol,标注物质聚集状态和对应反应的焓变写出热化学方程式;
②图象中甲烷体积分数随压强增大而增大,据此分析;
Ⅳ.(5)①二氧化碳和碳酸钾溶液反应生成碳酸氢钾;
②碳酸氢根离子存在电离平衡、氢氧根离子和碳酸氢根离子反应生成碳酸根离子。
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图2;
(1)硫化氢被硫酸铁氧化生成单质硫,过程i中H2S发生了氧化反应;
(2)过程Ⅱ是亚铁离子酸性条件下被氧气氧化生成铁离子,反应的离子方程式为:4Fe2++O2+4H+![]() 4Fe3++2H2O;
4Fe3++2H2O;
(3)Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全,分析30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率可知:工业脱硫应选择的最佳pH范围1.5≤PH<1.9,当PH大于1.9时,Fe3+开始沉淀,导致Fe3+、Fe2+离子浓度均下降,降低反应速率,PH<1.5时,TF菌活性较低,反应速率减慢;
Ⅱ.(4)①在催化剂的作用下,水蒸气将CH4氧化生成一氧化碳和水蒸气,图中反应的焓变△H=2582kJ/mol-2378kJ/mol=204kJ/mol,标注物质聚集状态和对应反应的焓变写出热化学方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+204kJ/mol;
②反应后气体物质的量增大,增大压强平衡逆向进行,图象中甲烷体积分数随压强增大而增大,据此分析,比较压强P1和P2的大小关系:P1>P2;
Ⅳ.(5)①将CO2和H2分离得到H2的过程示意图分析得到:二氧化碳和碳酸钾溶液反应生成碳酸氢钾,反应的离子方程式为CO2+H2O+CO32-=2HCO3-;
②HCO3-存在电离平衡:HCO3-![]() H++CO32-,阴极H+放电浓度减小平衡右移,CO32-再生,阴极反应:2H2O+2e-=H2↑+2OH-,OH-+HCO3-=CO32-+H2O,使碳酸钾溶液得以再生。
H++CO32-,阴极H+放电浓度减小平衡右移,CO32-再生,阴极反应:2H2O+2e-=H2↑+2OH-,OH-+HCO3-=CO32-+H2O,使碳酸钾溶液得以再生。

【题目】酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐加热来制取,该反应放热:

密度(g/mL) | 相对分子质量 | 颜色、状态 | 溶解性 | |
苯胺 | 1.04 | 93 | 无色油状液体 | 微溶于水, 易溶于乙醇、乙醚 |
乙酸酐 | 1.08 | 102 | 无色透明液体 | 遇水缓慢反应生成乙酸 |
乙酰苯胺 | 135 | 无色片状晶体, 熔点 114℃ | 不溶于冷水,可溶于热 水、乙醇、乙醚 |
实验步骤
①取5.00 mL苯胺,倒入100 mL锥形瓶中,加入20 mL水,在旋摇下分批加入6.00 mL 乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至150 mL烧杯中,加入适量水配制成 80 ℃的饱和溶液,再加入过量20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸3~5 min,_______,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品6.2 g。
请回答:
(1)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是______。
A 加20 mL水 B 旋摇下分批加入6.0 mL乙酸酐
C 玻璃棒将块状物研碎 D 充分搅拌
(2)在步骤②中对粗产品进行洗涤需要用到以下操作:
a 加入洗涤剂至浸没固体;b 洗涤剂缓慢通过;c 关小水龙头;d 开大水龙头; e 重复 2~3 次。
请对以上操作做出正确的排序__________。
(3)步骤③加入过量 20%的水的目的是________,横线处的操作步骤是_________。
(4)下列说法不正确的是______。
A 活性炭吸附有色物质,可以提高产率
B 冷却时,室温冷却比冰水浴冷却更易得到大颗粒晶体便于抽滤
C 抽滤用如图装置,为防止倒吸,结束时可先关闭水龙头,后打开活塞a

D 产品可放在表面皿上用热水浴烘干,烘干后可通过测量产品熔点判断产品纯度
(5)该实验的产率是___________。