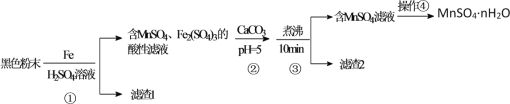��Ŀ����
����Ŀ����ƹ�ҵ����������ĵ����ˮ���������ˮʱ����������ĵ�����࣬������ຬ�ж��ֽ���(Ni��Cu��Fe��Cr��Al)����������Ͳ��������ʡ������Ǵ���ij�ֵ���������ͭ����Ԫ�ص�һ�ֹ�ҵ���̣�

������������������õ��Ľ���Һ�и���������Ũ�ȼ��±���
![]()
��1��������������У�Ϊ��߽������ʣ����Բ�ȡ�Ĵ�ʩ��___________(д������)��
��2���ڵ�����ͭ�Ĺ����У�Ϊ�����һ���ij���Ч��������Ƶ���ѹ�Դ�һЩʹFe2+�������������γ����к��е�����Ϊ___________��
��3��������ǰ��Ni2+Ũ�Ȼ������䣬��ʹNi2+�ڳ��ӹ��̲���ʧ������Һ��PO43-Ũ�Ȳ��ܳ���________ mol/ L��(�г��������ʽ��Ksp[Ni3(PO4)2]=5��10-31)
��4����Һ�е�___________�ɻ���ѭ��ʹ�ã��о����ֵ�NaOH��ҺŨ�ȹ���ʱ��������Ԫ�غ�Ԫ�ػ�����Һ�г��֣���Һ�г�����Ԫ�ص�ԭ��Ϊ________ (�����ӷ���ʽ����)��
��5��Ni(OH)2���������ص��������ϣ��ڼ��Ե�����У���س��ʱNi(OH)2��ΪNiOOH�����طŵ�ʱ�����ĵ缫��ӦʽΪ________��
��6�������ˮ�е�CrԪ��Ҳ�����������巨������ԭ��Ϊ�ڷ�ˮ�м��������FeSO4��������������Cr2O72-����ԭΪCr3+��ͬʱ����Fe3+�����������ǿ��������������(CrxFe3-xO4������д���������ǿ��������������(CrxFe3-xO4)���������ӷ���ʽ___________��
���𰸡����ȡ���������Ũ�ȡ������ FePO4��CrPO4��AlPO4 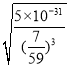 Na3PO4 Al(OH)3+OH-= AlO2-+2H2O NiOOH+H2O+e-=Ni(OH)2+OH- xCr3++Fe2++ (2-x) Fe3+ +8OH-=CrxFe3-xO4��+ 4H2O
Na3PO4 Al(OH)3+OH-= AlO2-+2H2O NiOOH+H2O+e-=Ni(OH)2+OH- xCr3++Fe2++ (2-x) Fe3+ +8OH-=CrxFe3-xO4��+ 4H2O
��������
��1������Ӱ�컯ѧ��Ӧ���ʵ����أ�������������У�Ϊ��߽������ʣ����Բ�ȡ�Ĵ�ʩ�м��ȡ���������Ũ�ȡ�����ȣ��ʴ�Ϊ���ȡ���������Ũ�ȡ�����ȡ�
��2�����ݳ�����������ܽ��Թ��ɣ���֪�������γ����к��е�������FePO4��CrPO4��AlPO4���ʴ�ΪFePO4��CrPO4��AlPO4��
��3������Ksp[Ni3(PO4)2]=5��10-31��ҪʹNi2+�ڳ��ӹ��̲���ʧ����ҪQc��Ksp[Ni3(PO4)2]����Һ��c(Ni2+)=7000mg/L=![]() mol/ L������Һ��PO43-Ũ�Ȳ��ܳ���
mol/ L������Һ��PO43-Ũ�Ȳ��ܳ���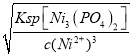 =
=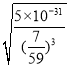 mol/ L���ʴ�Ϊ
mol/ L���ʴ�Ϊ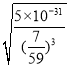 ��
��
��4�� ��������ͼ�����������ܽⲿ�ֳ��������ɵ�Na3PO4�ɻ���ѭ��ʹ�ã��о����ֵ�NaOH��ҺŨ�ȹ���ʱ��������Ԫ�غ�Ԫ�ػ�����Һ�г��֣���Һ�г�����Ԫ�ص�ԭ�����������ƽ����������ܽ⣬���ӷ���ʽΪAl(OH)3+OH-= AlO2-+2H2O���ʴ�ΪNa3PO4��Al(OH)3+OH-= AlO2-+2H2O��
��5�� Ni(OH)2���������ص��������ϣ��ڼ��Ե�����У���س��ʱNi(OH)2����������Ӧ����NiOOH�����طŵ�ʱ������NiOOH������ԭ��Ӧ����Ni(OH)2���缫��ӦʽΪNiOOH+H2O+e-=Ni(OH)2+OH-���ʴ�ΪNiOOH+H2O+e-=Ni(OH)2+OH-��
��6���ڷ�ˮ�м��������FeSO4��������������Cr2O72-����ԭΪCr3+��ͬʱ����Fe3+�����������ǿ��������������(CrxFe3-xO4�������������ǿ��������������(CrxFe3-xO4���������ӷ���ʽΪxCr3++Fe2++ (2-x) Fe3+ +8OH-=CrxFe3-xO4��+ 4H2O���ʴ�ΪxCr3++Fe2++ (2-x) Fe3+ +8OH-=CrxFe3-xO4��+ 4H2O��

����Ŀ��������Ϊ�����Դ���Ź㷺��Ӧ��ǰ����������Ȼ���Ʊ��������������¡�

��ش��������⣺
��.ת��������Ȼ��ѹ����������30��ʱ����T.F�������£����Ի������������ʾ��ͼ��ͼ��ʾ��
��1������i��H2S������___�����������ԭ������Ӧ��
��2������ii�����ӷ���ʽ��___��
��3����֪����Fe3+��pH��1.9ʱ��ʼ������pH��3.2ʱ������ȫ��
��30��ʱ����T.F�������£���ͬpH��FeSO4��Һ��Fe2+�������������±���
pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
Fe2+��������/��g��L��1��h��1�� | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
����������Ϣ���жϹ�ҵ����Ӧѡ������pH��Χ����˵��ԭ��___��
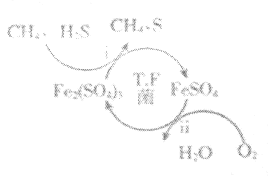
II.����ת�����ڴ����������£�ˮ������CH4�����������ͼ�ش����⡣
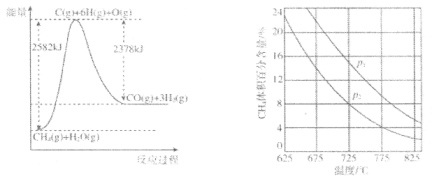
��4���ٸù��̵��Ȼ�ѧ����ʽ��___��
�ڱȽ�ѹǿp1��p2�Ĵ�С��ϵ��p1___p2��ѡ�>����<����������
III.CO�任��500��ʱ��CO��һ����ˮ��Ӧ����CO2��H2��
IV.H2�ᴿ����CO2��H2����õ�H2�Ĺ���ʾ��ͼ��ͼ��
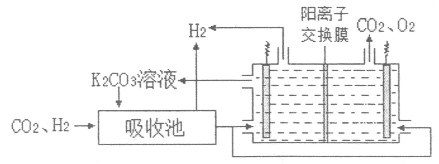
��5�������ճ��з�����Ӧ�����ӷ���ʽ��___��
�ڽ�ϵ缫��Ӧʽ������K2CO3��Һ������ԭ����___��
����Ŀ����a��b��c��d�ĸ������缫���йصķ�Ӧװ�ü����ַ�Ӧ�������£�
ʵ��װ�� | ����ʵ������ |
| a����������b���������� |
| b�������������c���ޱ仯 |
| d���ܽ⣬c����������� |
| ������ָʾ�ڵ����е�����a������d�� |
�ɴ˿��ж������ֽ����Ļ��˳���ǣ���������
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c