题目内容
8.氯元素的天然同位素有35Cl 和37Cl.氯元素的相对原子质量为35.45,则天然氯元素中35Cl 和37Cl的原子数目之比约为( )| A. | 3:1 | B. | 1:3 | C. | 3:2 | D. | 4:1 |
分析 氯元素的平均相对分子质量是由同位素的丰度计算出来的,同位素在自然界中的丰度,又称天然存在比,指的是该同位素在这种元素的所有天然同位素中所占的比例.
解答 解:设天然氯元素中35Cl 和37Cl的原子数目分别为x和y,依据题意有:$\frac{35×x+37×y}{x+y}$=35.45,解x:y≈3:1,故选A.
点评 本题考查物质的量及相对分子质量的计算,熟悉摩尔质量与相对分子之间的关系即可解答,较简单.

练习册系列答案
相关题目
9.下列物质中互为同分异构体的是( )
| A. | ${\;}_{6}^{12}$C与${\;}_{6}^{13}$C | B. | O2与O3 | ||
| C. |  和 和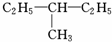 | D. |  和 和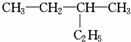 |
16.下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
| A. | 干冰和碘分别变为气体 | B. | 干冰和氯化铵分别受热变为气体 | ||
| C. | 二氧化硅和铁分别受热熔化 | D. | 食盐和葡萄糖分别溶解在水中 |
13.在反应:C(s)+CO2(g)=2CO(g)中,可使反应速率增大的措施是( )
①增大压强②升高温度③恒容通入CO2④增加碳的量⑤恒容通入N2.
①增大压强②升高温度③恒容通入CO2④增加碳的量⑤恒容通入N2.
| A. | ①②③⑤ | B. | ①②③④⑤ | C. | ①②③ | D. | ②③④ |
20.下列有关化学用语使用正确的是( )
| A. | NH4Br的电子式: | |
| B. | S2-的结构示意图: | |
| C. | 氚表示为:${\;}_{1}^{2}$D | |
| D. | 原子核内有l8个中子的氯原子:${\;}_{17}^{36}$Cl |
17.根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价,
部分短周期元素的原子半径及主要化合价,
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.075 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R,金属性L>Q | |
| B. | M与T形成的化合物具有两性 | |
| C. | L2+与R2-的核外电子数相等 | |
| D. | L的原子半径最大,电负性最小,T的原子半径最小,电负性最大 |
18.分类是化学学习中经常用到的方法,下列对一些物质或化学反应的分类以及依据正确的是( )
| A. | H2SO4是酸,因为H2SO4中含有氢元素 | |
| B. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间 | |
| C. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 | |
| D. | Na在Cl2中燃烧不是氧化还原反应,因为没有得氧或失氧 |
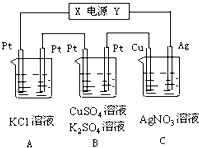 如图所示,若电解5min时铜电极的质量增加2.16g,B中一根Pt电极质量增加0.32g,且此时B中两极都有气体产生.试回答:
如图所示,若电解5min时铜电极的质量增加2.16g,B中一根Pt电极质量增加0.32g,且此时B中两极都有气体产生.试回答: