题目内容
3.氧化还原反应中实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-→NO↑+2H2OKMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生.
(1)写出并配平该氧化还原反应的离子方程式:3FeO+10H++NO3-=3Fe3++NO↑+5H2O
(2)若有0.3mol甲参加反应,标准状况下可生成NO2.24L.
分析 NO3-+4H++3e→NO+2H2O,该反应中硝酸发生还原反应,所以另一种物质必须具有还原性,只有FeO符合,与硝酸发生氧化还原反应生成NO和Fe(NO3)3,结合电子、电荷守恒配平,生成气体为NO,结合反应计算生成气体的体积.
解答 解:(1)NO3-+4H++3e→NO+2H2O,该反应中硝酸发生还原反应,所以另一种物质必须具有还原性,只有FeO符合,与硝酸发生氧化还原反应生成NO和Fe(NO3)3,反应的方程式为HNO3+FeO→Fe(NO3)3+NO↑+H2O,Fe元素的化合价升高,N元素的化合价降低,由电子、原子守恒可知,反应为10HNO3+3FeO=3Fe(NO3)3+NO↑+5H2O,离子反应为3FeO+10H++NO3-=3Fe3++NO↑+5H2O,
故答案为:3FeO+10H++NO3-=3Fe3++NO↑+5H2O;
(2)由反应可知,0.3molFeO反应生成0.1molNO气体,其体积为0.1mol×22.4L/mol=2.24L,故答案为:2.24;
点评 本题考查氧化还原反应及计算,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意从化合价的角度解答该题,难度不大.

练习册系列答案
相关题目
4.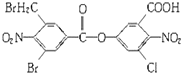 已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )
已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )
 已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )
已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )| A. | 6 mol | B. | 7 mol | C. | 8 mol | D. | 9 mol |
5.下列各组中的性质比较,不正确的是( )
| A. | 酸性:HClO4>HBrO4>HIO4 | B. | 沸点:H2O>HF>HCl>HBr | ||
| C. | 非金属性:F>O>S | D. | 稳定性:PH3<H2S<HCl |
18.合成氨工业中氢气可由天然气和水反应制备,其主要反应为:CH4(g)+2H2O(g)?CO2(g)+4H2(g)
已知,破坏1mol化学键需要吸收的热量如下表所示:
试通过计算判断,下列有关甲烷转化成氢气过程的能量变化示意图正确的是( )
已知,破坏1mol化学键需要吸收的热量如下表所示:
| 化学键 | C-H | O-H | C=O | H-H |
| 吸收热量(kJ/mol) | 414 | 464 | 803 | 436 |
| A. | 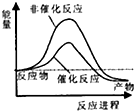 | B. | 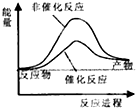 | C. | 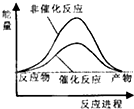 | D. | 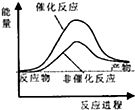 |
8.氯元素的天然同位素有35Cl 和37Cl.氯元素的相对原子质量为35.45,则天然氯元素中35Cl 和37Cl的原子数目之比约为( )
| A. | 3:1 | B. | 1:3 | C. | 3:2 | D. | 4:1 |
15.硒是第四周期ⅥA元素,现在含有元素硒(Se)的保健品已经进入市场,关于硒的说法中不正确的是( )
| A. | 原子序数为34 | B. | 还原性:H2Se<H2S | ||
| C. | 酸性:H2SeO4<HBrO4 | D. | Se氧化物化学式有:SeO2、SeO3 |
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 室温下,22.0g C18O2气体中含有的碳原子数目为0.5NA | |
| B. | 1mol OH-中电子数为10NA | |
| C. | 标准状况下,22.4L乙醇中含有的氧原子数为1.0NA | |
| D. | 1mol C2Cl6分子含有7 NA个共价键 |
13.在酸性溶液中,可大量共存的离子是( )
| A. | K+ Na+ OH- SO42- | B. | Mg2+ SO42- NH4+ Cl- | ||
| C. | K+ Na+ HCO3- Cl- | D. | K+ Na+ NO3- CO32- |